العلماء يصمِّمون أول خميرة تعمل بالطاقة الضوئية
تظهر التجاربُ السهولةَ التي يمكن للكائنات من خلالها تطوير قدرتها على تسخير ضوء الشمس للحصول على الطاقة
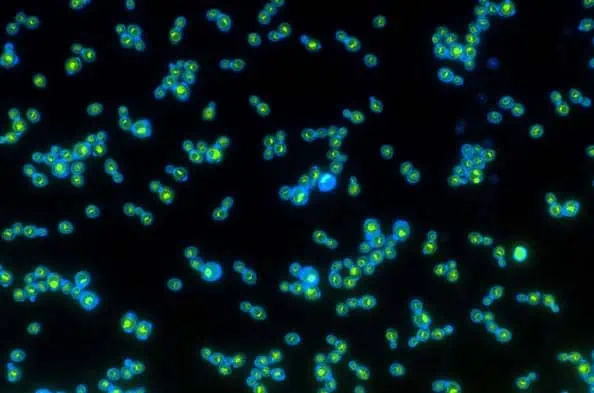
الخميرة Yeast من محبي الكربوهيدرات، تقتات بتخمير السكريات والنشويات من مصادر مثل العجين والعنب والحبوب، مع الخبز والشعير كمنتجات ثانوية مؤاتية. الآن، أوجد الباحثون نوعاً من أنواع الخميرة أقل اعتماداً على الكربوهيدرات، وذلك بتمكينه من استخدام الضوء كطاقة.
إن العمل، الذي تم الإبلاغ عنه في الأسبوع الأول من أبريل 2023 على الموقع bioRxiv، هو «الخطوة الأولى في أنماط أكثر تعقيداً من هندسة البناء (التمثيل) الضوئي الاصطناعي Artificial photosynthesis»، كما تقول ماغدالينا روز أوسبورن Magdalena Rose Osburn، عالمة الجيولوجيا الأرضية في جامعة نورث وسترن Northwestern University التي لم تشارك في البحث. كما أن البحث يلخص تحولاً تطورياً رئيسياً – تسخير الضوء. يقول فيليب سانتياغو تيرادو Felipe Santiago- Tirado، عالم بيولوجيا الخلايا الفطرية بجامعة نوتردام University of Notre Dame: «إنه أمر غير عادي… إلى حد ما، يبدو الأمر أشبه بتحويل حيوان إلى نبات».
لكن، ليس كذلك ليس تماما. لتحويل ثاني أكسيد الكربون إلى سكريات التي تُغذِّي الحياة على الأرض، تعتمد النباتات على مركب بروتيني يتضمن الكلوروفيل Chlorophyll لنقل الإلكترونات والبروتونات، التي تتفاعل كيميائيا وتنقل الطاقة. فقد عمل الباحثون لسنوات على إعادة إنشاء البناء الضوئي Photosynthesis لاستكشاف كيفية استخدام الضوء بشكل أكثر كفاءة كمصدر للطاقة في الألواح الشمسية والتطبيقات الأخرى ولمزاوجة النباتات Breed plants – والكائنات الأخرى – لتكون أكثر إنتاجية.
مركب الكلوروفيل يتطلب العديد من الجزيئات الأخرى للقيام بعمله. لذلك سعى أنتوني بورنيتي Anthony Burnetti، عالم الوراثة وعالم الأحياء التطوري في جورجيا للتكنولوجيا، ويليام راتكليف William Ratcliff – من معهد جورجيا للتكنولوجيا Georgia Institute of Technology – إلى حل أبسط. فقد ركزا على بروتين يعرف با رودوبسين Rhodopsin الذي لا يتطلب مجموعة جزيئية كبيرة. إنه حل استقرت عليه الطبيعة أيضاً: تستخدم البكتيريا – وبعض الطلائعيات Protists والطحالب البحرية وحتى فيروسات – الطحالب الرودوبسين لتحويل الضوء إلى طاقة قابلة للاستخدام، وغالباً لضخ البروتونات الضرورية للوظائف الخلوية.
أدخل الباحثان جين الرودوبسين من بكتيريا بحرية في خميرة الشعير (ساكاروميسيس سيرفييسي Saccharomyces cerevisiae) في طبق اختبار بتري. وكان بورنيتي يأمل بأن يجد الرودوبسين طريقه إلى حويصلة (الفجوة العصارية) Vacuole الخميرة، وهو كيس ممتلئ بالإنزيم الذي يحلل البروتينات غير الضرورية. ويغذي جزيء الطاقة المسمى أدينوزين ثلاثي الفوسفات Adenosine triphosphate (اختصاراً: الجزيء ATP) العملية عن طريق ضخ البروتونات في الفجوة لجعلها حمضية – مثالية للتحلل.
تساءل بورنيتي عما إذا كانت الطاقة الضوئية يمكنها القيام بهذه المهمة بدلاً من ذلك. ولكن جهود الفريق الأولى أخطأت عندما ذهب بروتين الرودوبسين الذي ينتجه الجين إلى عضيّة مختلفة معروفة ليس بتحليل البروتين بل بتخليقه. وبدلاً من ذلك، بحث بورنيتي عن الرودوبسين المعروف بالفعل بوجوده في الحويصلات. واستقر على استخدام واحد من الفطر الذي يؤدي إلى مرض تفحّم الذُرَة، وهو عامل مُمْرِض Pathogen من الفطريات. ومن خلال إضافة علامة فلورية Fluorescent tag إلى البروتين، تحقق هو وزملاؤه من أنه قد تم توطينه في حويصلة الخميرة، كما كانوا يأملون.
بعد ذلك، ذهبت طالبة الدراسات العليا أوتوم بيترسون Autumn Peterson، وهي عضو في فريق بورنيتي، إلى أبعد من ذلك لإثبات أن هذه الخميرة المهندسة كانت في الواقع تستخدم الضوء. فاستزرعت السلالة الجديدة في الطبق نفسه مثل الخميرة الأصلية غير المعدلة وعرّضتها للضوء الأخضر، وهو طول موجي يكون الرودوبسين أكثر حساسية له. ووجد الفريق أن الخلايا الموجودة في سلالة الاستشعار عن الضوء لها حياة أقصر لكنها تتكاثر بسرعة كافية لتتغلب على الخميرة غير المستشعرة للضوء بنسبة 0.8%. يقول سانتياغو تيرادو إنها «ميزة هائلة». بمرور الوقت، في الضوء، يتوقع بيترسون أن تحل الخلايا التي تستخدم الضوء في النهاية محل الخلايا غير المعدلة تماماً مثلما حلّت الكائنات الأولى المستخدمة الأولى محل منافسيها في الطبيعة بالدهور السحيقة.
يعتقد بورنيتي وزملاؤه أن الضوء يحفز رودوبسين على ضخ المزيد من البروتونات في الحويصلة، مما يخفف من حاجة الخلايا إلى إنفاق الجزيء ATP لهذه المهمة، وبدلاً من ذلك تُحرر الخلايا تلك الطاقة لمساعدة الخلية على النمو بطرق أخرى. وقد تؤدي زيادة حمضية الحويصلة إلى تقليلها خارج الحويصلة، مما يتسبب في عمل الإنزيمات الموجودة هناك بشكل أسرع وتحلّلها في وقت أقرب، وقد يساعد أيضاً على تفسير معدل الوفيات المرتفع بين هذه الخلايا المُعدَّلة. وبغض النظر عن الطريقة التي يعمل بها، «من الواضح أنه مفيد لخلايا الخميرة»، كما يقول مايكل ماكموري Michael McMurray، عالم البيولوجيا الجزيئية في الحرم الجامعي الطبي بجامعة كولورادو University of Colorado أنشوتز Anschutz Medical Campus.
ولكن التجربة ربما لا تكشف الكثير عن كيفية تطور استخدام الرودوبسين في الطبيعة. يقول روبرت بلانكينشيب Robert Blankenship، عالم الكيمياء الحيوية الفخري من جامعة واشنطن في سانت لويس Washington University in St.Louis: «أعتقد أن المؤلفين يبالغون في التأكيد على الأهمية الثورية لعملهم… هذا تركيب اصطناعي وليس نتاج تطور طبيعي».
يعتقد البعض الآخر أن العمل يمكن أن تكون له تطبيقات بحثية صناعية وطبية وأساسية. يقول ألاتين كايا Alaattin Kaya، عالم البيولوجيا الذي يدرس التقدم في العمر Aging في جامعة فرجينيا كومنولث Virginia Commonwealth University، إن خلايا الخميرة هذه يمكن أن تساعد على توضيح سبب تسبب تحمض الحويصلات على مدى حياة الخلية أحياناً عند حدوث خلل في الميتوكوندريا، ومن ثم تسريع الشيخوخة. وهو يود أن يضيف الرودوبسين إلى الميتوكوندريا نفسها لمراقبة تأثيره.
كما يرغب بورنيتي في استهداف الميتوكوندريا أيضاً، ولكن لسبب مختلف. «على الرغم من أنه يبدو أن ذلك لم يحدث قط بشكل طبيعي، فإننا نخطط فعليا لإدخال الرودوبسين في النهاية في الميتوكوندريا». نظراً لأن الميتوكوندريا يمكنها إنتاج الجزيء ATP، فإن إضافة رودوبسين يمكن أن توفر الكثير من الطاقة مباشرة من الشمس، تماماً كما يفعل البناء الضوئي. وبذا، ستكون الخميرة أقرب إلى النباتات.
بقلم: إليزابيث بانيسي
ترجمة: Google Translate
تنقيح: فريق تحرير مجلة العلوم
©2023, American Association for the Advancement of Science. All rights reserved





