تعطُّشنا للمياهِ يجعلُ المحيطاتِ أكثرَ ملوحةً
قد يكون الخيار الوحيد للحصولِ على مياه نظيفة مع تنامي الحاجة إليها هو من محيطاتنا، ولكن هنالك ثمناً لذلك.

بقلم: كاثرين بورزاك Katherine Bourzac
ترجمة: آية علي
شرح الصورة: المحيط يُمثل للمجتمعات الساحليّة مصدرا مغريا للمياهشرح الصورة: المحيط يُمثل للمجتمعات الساحليّة مصدرا مغريا للمياه
نجت مدينة كيب تاون في الوقت الحالي من إحدى الكوارث بأعجوبة. فبعد شهور من جفافٍ لا هوادة فيه، بدأت الأمطار الشتوية الأخيرة بإعادة ملء سدودها الظمأى. وهذا لا يعني أنّ الأمور متيسّرة، إذ لا يزال استخدام سكان المدينة للمياه مقتصرا على خمسين لترا من المياه يوميا، وهي كمية بالكاد تكفي لملء حوض استحمام حتى منتصفه. ولكنهم تمكّنوا على الأقل من تفادي الأيام صفر، وهي الأيام التي تنفد فيها المياه من الصنابير ويضطرون إلى الانتظار في طابور لجمع حصص من بقايا المياه.
تُعتبر هذه المدينة في جنوب إفريقيا مثالا متطرفا، ولكنّها ليست المكان الوحيد الذي يواجه نقصًا حادًّا في المياه. وتتوجه عدة مدن نحو المحيطات لتخطّي هذا العطش، والتي تبدو لنا، في ظاهرها، مصدر مياه لا ينضب. فهي تقوم بذلك من خلال تحلية المياه Desalination، وهي تقنية لتنقية المياه موجودة منذ عقود. وتعمل كيب تاون في عجالة على تشغيل عدة محطات لتحلية المياه، كما يجري إنشاء العديد من المحطات في أماكن أخرى. ولكن انتشار هذه المحطات جعل الاهتمام يتركّز على ما تخلّفه وراءها، وهو ملايين اللترات يوميا من محلول ملحي مركّز.
ويدعو العلماء الآن إلى توخي الحذر بشأن عواقب إغراق كل هذا الملح في البيئة. وتقول المهندسة إيمي تشايلدريس Amy Childress: “الملوحة المتزايدة واحدة من أهمّ القضايا البيئية في القرن الواحد والعشرين.” ولكنّ هنالك أساليب أكثر ذكاء للتحلية بدأت بالظهور، وفوائدها لا تقتصر البتّة على توفير مياه نظيفة.
ساو باولو، القاهرة، بكين، بانغالور؛ تطول قائمة المناطق التي تعاني نقصاً في المياه، وهي قضية تلامس كلّ قارّة. وحتى لندن التي غالبًا ما يُنظر إليها كمدينة رطبة لا تحصل إلا على 600 ملليمتر من الأمطار سنويًا، ويُحتمل أن تواجه مشكلات في الإمداد بحلول عام 2025. ومن المحتّم أن تتفاقم الأمور مع تنامي عدد السكان، ففي عام 2007، وجدت الأمم المتحدة أن نحو 1.6 بليون شخص يفتقرون إلى البنية التحتية الكافية لتزويدهم بمياه الشرب، كما تتوقّع المنظّمة أنه بحلول عام 2050 فإنّ 1.8 بليون شخص (أي ما يقرب من ربع سكان العالم) سيعيشون في مناطق لا يوجد فيها ما يكفي من المياه لإبقائهم على قيد الحياة.
ستكون الطريقة المثلى لتلبية الطلب هي من خلال الاستفادة من مخازن المياه العذبة، كالأنهار والخزانات الممتلئة بمياه الأمطار، أو ربّما آبار المياه الجوفيّة. ولكن هنالك الكثير من الأماكن التي لا تمتلك مصادر مياه كافية ويسهل الوصول اليها من أجل إمداد أعداد السكان المتنامية. وأحد الخيارات المتاحة لحل هذه المشكلة هو إعادة تدوير مياه الصرف على نطاق بالغ الضخامة. ومن الخيارات الأخرى أيضا اللجوء إلى المياه المالحة، كالمحيطات أو البحيرات المالحة.
وهنا يأتي دور تحلية المياه، وهنالك الكثير من الطرق للقيام بذلك. ويمكننا مثلا تبخير المياه من مكان معين وتكثيفها في مكان آخر، مخلّفة وراءها الملح والشوائب. ولكن أكثر الطرق كفاءة من حيث استخدام الطاقة هي التناضح العكسي Reverse osmosis.

ثماني محطات لتحلية المياه قيد الإنشاء في كاليفورنيا.
تخيّل وجود محلول ملحي قوي، وآخر ضعيف، يفصلهما غشاء لا يسمح سوى بمرور الماء. وسيتدفق الماء في هذه الحالة من المحلول الضعيف إلى المحلول القوي بصورة طبيعية، موازنا بين التركيزين في عملية تسمى التناضح. افعل العكس، واَجبر مياه المحيطات باستخدام الضغط العالي على المرور إلى الاتجاه المعاكس عبر غشاء يستثني الملح، وستكون على الطريق الصحيح لصنع مياه صالحة للشرب.
صار هذا النهج أكثر شيوعا، ففي عام 2005، أنتجت محطات التحلية نحو أربعين بليون لتر من المياه يوميًا، وذلك وفقًا لرابطة التحلية الدولية International Desalination Association. وارتفعت هذه الكميّة بحلول عام 2015 إلى 87 بليون لتر أنتجتها ما يقرب من 1900 محطّة حول العالم. وتقع الغالبية العظمى من هذه المحطّات في البلدان الجافة حول الخليج العربي، ولكنّ انتشار التقنية في ازدياد في أماكن أخرى كذلك. وتحصل مدينة أديلايد Adelaide الأسترالية على ما يقرب من نصف مياهها من محطّة تحلية ضخمة، كما تمتلك كاليفورنيا بالفعل بعض المحطّات، وتنفق أكثر من ثلاثين مليون دولار على ثماني محطات جديدة.
وكلّ هذه أخبار رائعة، باستثناء أمر واحد: ما الذي سنفعله حيال كلّ هذه المخلّفات من المحلول الملحي؟ تبلغ ملوحة هذه المياه ضِعْف تلك التي بدأنا بها، بناء على تقنية التحلية المستخدمة، وتتخلص منها معظم المحطات عبر ضخّها إلى البحر مرّة أخرى. هذا هو مصدر قلق الباحثين، بمن فيهم تشايلدريس من جامعة جنوب كاليفورنيا University of Southern California.
يتباين تركيز الأملاح في البحر، ولكنه يكون 35 جزءاً من الألف في المتوسّط، أيّ أنّ كل ألف جرام من مياه البحر تحتوي على نحو 35 جراماً من الملح. وبمجرد أن تتجاوز مستويات الملح المستوى الصالح للنباتات والحيوانات البحرية، يكون هنالك خطر من أن تتوقف خلاياها عن العمل بشكل صحيح.
والأدلة الحالية حول ما يحدث للحياة المحيطة بالمياه المالحة المتدفقة من محطات التحلية أدلة مختلطة. ففي عام 2012 بحثت دراسة لمجلس ولاية كاليفورنيا لمراقبة الموارد المائية California State Water Resources Control Board في كيفية استجابة الحيوانات لتركيزات الملح المتزايدة في ظروف مختبرية. ووجدت هذه الدراسة أن العديد من الأنواع البحرية قد تكون بخير في الملوحة الزائدة، ولكن بعض الأنواع المهمّة، كطحلب الكِلْب العملاق Giant kelp، قد تكون في خطر. وتشكّل الخيوط الكثيفة من هذه الطحالب الشاهقة غابات تحت الماء على طول ساحل كاليفورنيا، وتعد مظلّاتها موطناً لمجموعة متنوعة من الأنواع بما في ذلك ثعالب البحر وقنافذ البحر.
ويقول مايكل فوستر Michael Foster من معامل موس لاندنج مارين Moss Landing Marine Laboratories في كاليفورنيا إن طحلب الكِلْب العملاق يتكاثر بنجاح باهر في مستويات ملوحة تتراوح بين 25 و35 جزءاً من الألف. ومع بلوغ ملوحة المحيط الهادي 35 جزءاً من الألف بالفعل، فإنّ أيّ زيادة قد تكون مشكلة بالنسبة إلى الطحلب وللنظام الإيكولوجي الذي يدعمه. كما توصّلت دراسة مجلس مراقبة المياه كذلك إلى أن حلزون أذن البحر الأحمر Red abalone، وهو حيوان رخوي صالح للأكل، يبدو شديد الحساسية للزيادات في الملوحة.

شرح الصورة: تأثير المخلفات الملحية في غابات عشب البحر غير معروف.
ريتشارد هيرمان Richard Herrmann/FLPA
وتحذّر هيذر كولي Heather Cooley، مديرة الأبحاث من معهد المحيط الهادي Pacific Institute، وهي مؤسسة أبحاث مائية في كاليفورنيا، من العواقب غير المقصودة للتخلص من المياه المالحة، وتعقّب قائلة: “إنّنا لا نعرف حقا ماهيّة آثار ذلك في البيئة البحريّة.”
وكانت كولي قد أجرت مراجعة موسّعة للأدلّة، كالنظر إلى مستويات التنوّع الحيوي والأكسجين المذاب قبل وبعد تركيب مصارف المخلفات الملحية من محطات التحلية في مدينة بيرث بأستراليا، وفي أماكن أخرى. ولم تكن النتائج سهلة التفسير، وهي لا تنطبق بالضرورة على أماكن أخرى. وتقول كولي إنّ أنماط الأمواج مثلا تؤثر في تشتّت هذه المحاليل الملحية.
ومع ذلك، تعني المخاطر المحتملة أن على معظم محطات تحلية المياه تخفيف المخلّفات الملحية قبل تصريفها في المحطات. وهذا في حد ذاته يعتبر إشكاليّة. وغالبا ما تكون المواد المستخدمة للتخفيف هي إمّا مياه صرف مُنظَّفة أو مياهاً مستخدمة لتبريد المنشئات الصناعيّة. فهي نظيفة بالقدر الذي يسمح لنا بتفريغها في المحيطات، ولكنها غير صالحة للشرب.
“إنّ عملية التحلية المثالية هي التي ستقتنص المعادن الثمينة أيضا، وليس المياه فقط.”
وهذا الإجراء بأكمله غارق في التناقضات، فحاجتنا إلى محطات التحلية تكون في حالة النقص في المياه العذبة فقط، ومع ذلك فهي تأخذ المياه العذبة التي يمكن تنظيفها بسهولة لجعلها صالحة للشرب، وتصرفها بدلا من ذلك في البحر. وتقول كولي: لماذا لا نعيد استخدام المياه؟ هل نعالجها ثم نعيد تصريفها إلى البحر مع المخلفات الملحيّة لمحطات التحلية؟ إنّه لأمر ينافي المنطق.”
وتعتقد تشايلدريس أن الهندسة الإبداعية قادرة على وضع حد لهذا الأمر. علينا، من أجل تحلية المياه، أن نحارب نزعتها الطبيعية للتدفق من مناطق ذات التركيز الملحي المنخفض إلى تلك عالية التركيز. ولكن إذا تركت الطبيعة تأخذ مجراها في التناضح، أي نحو الأمام وليس الخلف، فقد نتمكن من جعل المزيد من المياه تتدفق عبر غشاء يستثني الملح إلى حاوية من المحلول الملحي ممّا يزيد من الضغط. ويمكن استخدام هذه المياه المضغوطة لتشغيل التوربينات وتوليد الطاقة، في عمليّة تسمّى التناضح الأمامي بالضغط pressureretarded forward osmosis (PRFO). أضِف هذه المرحلة إلى محطة لتحلية المياه بالتناضح العكسي، ولن تخفّف لك المخلفات الملحية فحسب، بل ستحصل كذلك على طاقة يمكن إعادتها مرة أخرى إلى العملية، أو استخدامها كيفما تشاء (انظر: الرسم التوضيحي حل التخفيف).
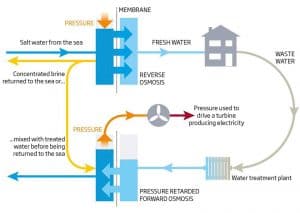
حل التخفيف Dilution solution
تنتج عملية تحلية المياه محاليل ملحية مركزة، ويمثّل ضخها مرة أخرى الى البحر مشكلة محتملة للبيئة، ولكن تخفيفها يهدر المياه التي كانت سيعاد تدويرها بدلا من ذلك. وربما يسهم استخراج الطاقة من عملية التخفيف في جعل الأمر مجديا.
*مياه مالحة من البحر – الضغط/ التناضح العكسي – الغشاء – مياه عذبة – مخلفات المياه – محطة لمعالجة المياه – التناضح الأمامي بالضغط
محاليل ملحية مركزة تعاد الى البحر/ أو تخلط مع المياه المعالجة قبل تصريفها في البحر –
الضغط – الضغط المستخدم لتشغيل التوربينات وتوليد الكهرباء.
لم تتمكّن هذه الأنظمة الهجينة من العمل على نحوٍ جيّد حتى الآن، وقد أُغلِقت أول منشاة من هذا النوع كانت قد افتتحت عام 2009 بإدارة الشركة النرويجية ستاتكرافت Statkraft بعد خمس سنوات من افتتاحها لكونها لم تُولّد ما يكفي من الكهرباء لتبرير البناء وتكاليف التشغيل. وتعمل تشايلدريس في الوقت الحالي على نمذجة أنظمة مماثلة في مختبرها لمعرفة ما إذا كان تحقيق نجاحها ممكنا، على الرغم من أن التفاصيل لا تزال طيّ الكتمان.
ولكن هنالك بوارق أمل في أماكن أخرى، إذ يقول نيل تايشونغ تشونغ Neal TaiShung Chung، المهندس الكيميائي من جامعة سنغافورة الوطنية National University of Singapore، إنّ مختبره طور هذه التقنية إلى درجة تجعلها معقولة من الناحية الاقتصادية. ويأتي هذا الأمر في أوانه تماما، “فنحن لا نملك الطاقة ولا المياه،” على حد تعبير تشونغ. وتشتري سنغافورة كميات كبيرة من المياه من جارتها ماليزيا، ولكن من المقرر انتهاء الترتيبات خلال خمسة وثلاثين عاما، ويشكّل هذا الأمر صراعا سياسيا منذ فترة طويلة.
لقد أنشأ فريق تشونغ نظام اختبار يعتمد على الفكرة الأساسية نفسها التي وظّفتها محطة ستاتكرافت، ولكن باستخدام الأغشية المُحسّنة التي طوّرها الفريق. وعندما شغل الباحثون هذا النظام لمدة 500 ساعة، مع تزويده بمياه الصرف البلدية ومياه البحر، لم يتجاوز استهلاكه للطاقة واطا واحدا للمتر المُكَعّب من المياه المحلّاة، أي ربع الكمية المطلوبة في العادة لعملية التناضح العكسي وحدها. وقد ابتاعت حاضنة بحثية للمشاريع الجديدة في سنغافورة التصاميم، وتخطّط لإنشاء محطّة تجريبية أكبر.
يوتوبيا مُطلَقة
يرغب البعض في أن يأخذ مسألة التحلية إلى ما هو أبعد من ذلك. وقد استمر بإزالة الماء من المحلول الملحي وستحصل في النهاية على الماء النقي والملح. وتطلق تشايلدريس على هذا الأمر “يوتيوبيا مُطلقة”، أمّا الاسم التقني له فهو: تحلية المياه صفريّة التفريغ للسائل Zero liquid discharge desalination (اختصارا: التقنية ZLD). وسيحصل من ينجح في فعل هذا الأمر على مكافئة ثلاثيّة الجوانب: صفر مياه مالحة، حدًّا أقصى من المياه العذبة، ومجموعة من المركّبات القيّمة. وتشمل هذه المكوّنات في بعض الحالات على أملاح الليثيوم، والتي من شأنها توفير العنصر الحاسم لأفضل بطاريات لدينا.
ويقول كريستوفر بيلونا Christopher Bellona، وهو مهندس بيئي من جامعة كولورادو للمعادن Colorado School of Mines: “إنّ كمية العمل الكبيرة المنجزة في هذا المجال مذهلةٌ للغاية.” وقد استكشف الكيميائيون أي نوع تقريبا من المعادن المستخرجة من المحاليل الملحية، كاليورانيوم والليثيوم والروبيديوم وملح الطعام العادي. ولكن تحويل المخلفات الملحية إلى كنوز لم يسبق له النجاح والانتشار، ويرجع هذا في الأساس إلى وجود الأملاح المختلفة بتركيزات منخفضة، وضمن تركيبات يصعب فصلها، ولكن هنالك عدداً قليلاً من الأماكن التي تصل في المُحصّلة إلى الجدوى الاقتصادية.
وتحدث معظم عمليات تحلية المياه في الساحل، ولكن الولايات المتحدة مستثناة من ذلك. وهنالك الكثير من احتياطات المياه الجوفية التي تميل إلى الملوحة في الكثير من المناطق، وهذا هو السبب وراء كون 95% من محطات التحلية فيها داخلية. وتمثل المخلفات الملحية مشكلة أكبر من المعتاد في هذه الحالة، وذلك لعدم وجود محيطات لتصريفها فيها، لذا غالبا ما يُتخلَّص منها في الأنهار. كما قد يجري تحويل الأراضي رخيصة الثمن الى أحواض للتبخير. أما في ولاية تكساس، وفي الأماكن الأخرى ذات الجيولوجيا المواتية؛ فإنّها تُحقن في آبار عميقة. ولكن كل هذه الخيارات لديها قدرات محدودة، لهذا السبب تحاول ولاية أريزونا الحصول على تصريح من المكسيك لبناء قناة تحمل المياه المالحة إلى البحر، ومساعيها هذه لم تُكلَّل بالنجاح حتى الآن.
وتعدّ محطّة كاي بايلي هوتشيسون Kay Bailey Hutchison في مدينة إل باسو El Paso بولاية تكساس أكبر مرفق للتحلية الداخلية للمياه في الولايات المتحدة. إنّها تروي عطش 2.7 مليون شخص، وتحقن محلولها الملحي في آبار عميقة. وتعد هذه العملية مكلفة للغاية، وستمتلئ الآبار عمّا قريب، وهما أمران ضخّا حياة جديدة في شرايين حلم تحلية المياه صفريّة التفريغ للسائل (التقنية ZLD). وقد تعاونت المحطة مع شركة Enviro Water Minerals في إل باسو، وتمخّض عن هذا التعاون اكتمال بناء منشأة لتعدين المخلفات الملحية في شهر إبريل، وهي منشأة مستوحاة من صناعة النفط وتستخدم بعض التقنيات الخاصة بها. ويصف هابل هاوسمان Hubble Hausman، الرئيس التنفيذي للشركة، هذه المنشأة بأنها “مصفاة لتكرير المياه.” فمثلما نستطيع فصل النفط الخام إلى العديد من المنتجات القيّمة، تفصل هذه المنشأة المحاليل الملحية إلى خمسة تيارات مختلفة مما يؤدي في المحصلة إلى استخراج كل الماء تقريبًا، وحفنة من المركبات المفيدة. وتشمل هذه المواد حمض الهيدروكلوريك وهيدروكسيد الصوديوم والجبس وهيدروكسيد المغنيسيوم، وجميعها مواد تستخدم في الصناعة أو في مواد البناء.
وسوف تعمل المنشأة بكامل طاقتها قريبا، حيث ستستعيد يوميا 7.5 مليون لتر إضافي من مياه الشرب من المحطّة. ولا تضم المنشأة تقنيات جديدة، كل ما في الأمر تشكيل تراكيب جديدة لتقنيات موجودة بالفعل. ويقول مايكل ميكلي Michael Mickley عن هذا الأمر، وهو عالم هيدرولوجي ومستشار في كولورادو: “هذه فكرة عبقريّة، ولكن السؤال هو: هل ستكون مُجدية من الناحية الاقتصادية؟”
كنزٌ نفطيٌّ دفين
يبحث مهندسون آخرون في مسألة تحويل مخلفات المياه إلى كنز في ظلِّ ظروفٍ أكثر صعوبة. ويبدي بيني فريمان Benny Freeman من جامعة تكساس في أوستن اهتمامه بآبار النفط، والتي تُخرج كمية مياه تفوق النفط المستخرج منها بخمسة أضعاف. ويعقّب على هذا قائلا: “هنالك محادثات حول استخدام المياه، ولكن أقلّ ما يمكننا فعله هو إعادة ضخّها إلى باطن الأرض.”
ومع ذلك، تحتوي مياه آبار النفط في تكساس على 1000 جزء في المليون من الليثيوم. وكان فريمان قد تعاون مع كيميائيين من جامعة موناش Monash University في أستراليا لتطوير أغشية يمكنها فصل العناصر عن الماء على نحوٍ انتقائي. وحتى إن كان تعدين الليثيوم بهذه الطريقة مُجديا من الناحية الاقتصادية، فإنّ فريمان هو أوّل المعترفين بأنّ تحويل هذا النظام إلى عملية كاملة لتحلية المياه سيمثّل تحديا، ولكنّه يقول إن من الواضح أنّه سيكون تجربتنا القادمة.”
ولن ينجح تحقيق حلم التقنية ZLD في كل مكان، ولكن تحلية المياه عبارة عن أداة يتعيّن على مخطّطي المدن والدول الاستعداد لها، وذلك على حد تعبير تشايلدريس. وتضيف أن الطريقة الوحيدة لحل المشكلات التي تأتي معها هي تبنّي مجموعة متنوعة من التقنيات، وانتقاء الخيارات التي تصلح محليًا. ويرجع السبب في عدم استخدام العديد من هذه الأفكار المتطورة على نطاق واسع إلى “أنّنا لسنا يائسين بما فيه الكفاية بعد،” وليس لأنّها لا تعمل. ربما تكون العبرة التي علينا أخذها من كيب تاون هو أنّنا قد نكون كذلك عمّا قريب.
كاثرين بورزاك Katherine Bourzac: صحافية مستقلة تعمل في مجال العلوم في ولاية سان فرانسيسكو.
نشرت المقالة في مجلة نيوساينتيست، العدد 3194، 8 سبتمبر 2018.





