بدء تجارب لإيجاد سلاح جديد ضد داء باركنسون: الضوء
قال المرضى بفوائدها، إلا أنه من غير الواضح الكيفية التي يحمي بها الضوء القريب من الأشعة تحت الحمراء خلايا الدماغ، وعلماء يشكون في ذلك
بقلم: جنجان سينها
ترجمة: مي بورسلي
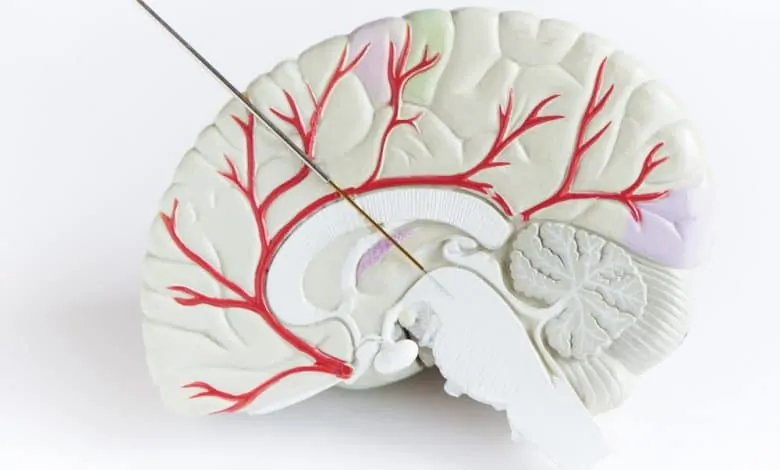
قد يساعد العلاج بالضوء Light therapy على تحسين الحالة المزاجية والتئام الجروح وتقوية جهاز المناعة. لكن، هل يمكنه تحسين أعراض داء باركنسون Parkinson’s disease أيضًا؟ تجربة هي الأولى من نوعها من المقرر إطلاقها في خريف 2020 بفرنسا، تهدف إلى معرفة ذلك. ففي سبعة مرضى سينقل كابل الألياف البصرية Fiber optic cable المزروع في أدمغتهم نبضاتٍ من ضوء الأشعة القريبة من تحت الحمراء Near infrared pulses (اختصارا: الضوء NIR) مباشرة إلى المادة السوداء Substantia nigra، وهي منطقة عميقة في الدماغ تتدهور عند الإصابة بمرض باركنسون. والفريق الذي يقوده عليم لويس بن عبيد Alim-Louis Benabid، من معهد كليناتيك Clinatec Institute – وهي شراكة بين العديد من معاهد الأبحاث الممولة من الحكومة والصناعة – يأمل بأن يحمي الضوءُ الخلايا في تلك المنطقة من الموت.
هذه الدراسة هي واحدة من مجموعة دراسات لاستكشاف الكيفية التي يمكن للمرضى المصابين بداء باركنسون الاستفادة من الضوء. ويقول دون باورز Dawn Bowers، الاختصاصي بعلم النفس العصبي من كلية الطب في جامعة فلوريدا of the University of Florida College of Medicine، والذي يُجري تجربة على المرضى تُبث فيها نبضات من الضوء NIR عبر الجمجمة بدلاً من إيصالها إلى الدماغ عبر وسط مزروع: “إنني متحمس جدا”.
والدراسات المحدودة التي أُجريت على المصابين بداء باركنسون وعلى نماذج حيوانية للداء كانت قد أشارت بالفعل إلى وجود فوائد، لكن بعض الباحثين في التيار السائد من دراسة داء باركنسون يشكون في ذلك. فلم يوضح أحد بالضبط الكيفيةَ التي يمكن بها للضوء أن يحمي الخلايا العصبية Neurons الرئيسية – أو لماذا يجب أن يكون له أي تأثير على الإطلاق في الخلايا المدفونة بأعماق الدماغ التي لا ترى ضوء النهار أبدًا. ويقول المشككون إن معظم، أو كل الإشارات المشجعة التي شوهدت حتى الآن في الأشخاص، قد تكون نتيجة للتأثير الغفل (الوهمي) Placebo effect. ونظرًا لعدم وجود مؤشرات حيوية ترتبط جيدًا بالتغيرات في أعراض داء باركنسون “فإننا نعتمد على مراقبة السلوك”، كما يقول ديفيد سولزر David Sulzer، الاختصاصي بعلم البيولوجيا العصبية من مركز إيرفينغ الطبي بجامعة كولومبيا Columbia University Irving Medical Center، ومحرر مجلة باركنسون ديزيز أن بي جي npj Parkinson’s Disease. ويتابع قائلا: “ليس من السهل الحماية من التأثيرات الغفل”.
ولكن المؤيدين يشيرون إلى علاج داء باركنسون باستخدام التحفيز العميق للدماغ Deep brain stimulation (اختصارا: التحفيز DBS)، الذي تتعرض فيه مناطق الدماغ المصابة لتيار كهربائي بتردد معين. وقد صار التحفيز DBS الذي اخترعه ابن عبيد قبل أكثر من 30 سنة إجراءً قياسيًا لعلاج الرعاش وغيرها من الأعراض الحركية الشديدة في مرضى باركنسون، على الرغم من أن طريقة عملها ليست واضحة تمامًا أيضًا. ويقول مايكل هامبلين Michael Hamblin، الباحث من مركز ويلمان للطب الضوئي في مستشفى ماساتشوستس العام Wellman Center for Photomedicine at Massachusetts General Hospital، إن تأثير الشفاء الموثق جيدًا للعلاج بـ ‘الليزر منخفض مستوى التردد’ في الأنسجة الأخرى أمر مشجع. وفي بعض الدول يستخدم الأطباء الليزر روتينيا لعلاج الألم أو تسريع التئام الجروح.
قبل عشر سنوات أُلهِم جون ميتروفانيس John Mitrofanis، الاختصاصي بعلم التشريح العصبي من جامعة سيدني University of Sydney، لتجربة الضوء على الباركنسون بعد أن أخبره زميله أن الضوء NIR يحمي خلايا الشبكية Retinal cells من السموم. وفي عام 2012 أظهر فيها هو، مع زملائه في دراسة أجريت على نموذج من فئران مصابة بداء باركنسون، أن الضوء NIR الموجّه إلى رأس الفأرة يحمي الخلايا المنتجة للدوبامين Dopamine-producing في المادة السوداء من السم العصبي.
“أنا متشكك، حتى وإن كنت أعتقد أيضًا، أن هذا مجال مثير يستحق البحث فيه” “أنا متشكك، حتى وإن كنت أعتقد أيضًا، أن هذا مجال مثير يستحق البحث فيه” ديفيد سولزر، من مركز إيرفينغ الطبي في جامعة كولومبيا
فاتصل ميتروفانيس الذي أخذه الحماس بذلك الوقت بابن عبيد الذي أمضى معه عامًا في دراسة التحفيز DBS. ويتذكر ميتروفانيس قائلا: “ابن عبيد – بصفته الجراح- قال لنا: علينا تطوير جهاز ضوئي يقترب من المنطقة”. وقد استنتج الباحثون أن الضوء الساطع من خارج الجمجمة لن يخترقها إلى العمق الكافي لإحداث فرق في الإنسان والحيوانات الكبيرة.
وفي عام 2017 حقن هو، مع زميلته الباحثة سيسيل مورو Cecil Moro، 20 نسناسًا من نسانيس المكاك Macaques بسمٍ عصبي معروف بأنه يسبب أعراض داء باركنسون. وفي تسعة منها أوصلوا الضوء NIR إلى المنطقة الوسطى من الدماغ من خلال جهاز مزروع. ويتذكر ميتروفانيس الكيفية التي عولج بها أول نسناس بالضوء NIR، والتي أدت إلى تعافيه بعد ثلاثة أسابيع من العلاج: “كان يتحرك وكأنه معافى. نظرنا إلى بعضنا البعض وتعانقنا. … وابتهجنا”. وعموما، ظهرت أعراض أقل على النسانيس المعالَجة بالضوء NIR من المجموعة غير المعالَجة واحتفظت بنسبة أكثر بـ 20% إلى 60% من خلايا الدماغ المستهدفة بالسم العصبي.
هذا، وقد تعاون ميتروفانيس أيضًا مع كاثرين هاميلتون Catherine Hamilton، وهي طبيبة مهنية متقاعدة في تسمانيا عالجت ركبتها المصابة بالتهاب المفاصل من خلال لفها بصمامات ثنائية ضوئية Light-emitting diodes (اختصارا: الصمامات LED). وفي عام 2019 نُشرت دراسة أجريت على ستة مرضى باركنسون أفادت فيها هاملتون وميتروفانيس وآخرون بأن ارتداء خوذة مبطنة بالصمامات LED تُحسِن من تعبيرات الوجه والسمع والمشاركة في المحادثات ونوعية النوم والدافعية، على الرغم من أنه لم يكن له تأثير كبير في الأعراض الحركية. ويقول آلان مينسون Alan Minson، والذي يعاني الباركنسون ويعيش في لونغفورد بأستراليا، والذي بدأ باستخدام الخوذة في يوليو 2019: “إذا فاتتني جلسة ليوم واحد، فهناك تغيير تدريجي في نفسيتي… فتعود الأحلام السيئة، ويقل صبري ويزداد خمولي”. أما آن ليبرت Ann Liebert، من جامعة سيدني؛ فتخطط لإجراء دراسة على 120 مريضًا باستخدام خوذة أكثر تطوراً. وفي جهود مماثلة سيختار باورز 24 مريضًا عشوائيًا لتطبيق الضوء NIR خارجيًا أو الضوء ( العلاج ) الغفل ورصد الفوائد السلوكية والحركية.
كما سيبحث باورز أيضًا عن علامات تدل على أن الضوء، كما اقترح البعض، يعزز الميتوكوندريا Mitochondria المنتِجة للطاقة في خلايا الدماغ. وقد أظهرت التجارب في أنبوب الاختبار أن الضوء قد يحفز إنزيم السيتوكروم سي أوكسيديز Cytochrome C oxidase enzyme، الموجود على أغشية الميتوكوندريا، لزيادة إنتاج الطاقة الخلوية، والتي بدورها قد تزيد من تدفق الدم وتحفز الخلايا، على إنتاج العديد من البروتينات الواقية للأعصاب وعوامل النمو. ويقول باورز: “لكنني لست مقتنعًا بأن جهازًا يوضع على الجمجمة يمكنه الاختراق بعمق كافٍ لإظهار تحسينات جوهرية”. وهي أكثر تفاؤلاً بتجربة ابن عبيد.
فهذه الدراسة ستتابع 14 مريضًا في مرحلة مبكرة من داء باركنسون لمدة أربع سنوات، سيخضع سبعة منهم إلى علاج دوري بضوء ذي نبضات من 670 نانومترا من الضوء توصل إلى الدماغ عبر كابل رفيع من الصمام الثنائي الليزري. ولن تجرى أي عملية جراحية على المرضى السبعة الآخرين؛ إذ حكم مجلس المراجعة الأخلاقية بعدم إخضاعهم لعملية جراحية لن تقدم أي فائدة. ويقول ابن عبيد إن الهدف الرئيس هو إثبات أن الغرسة آمنة، لكن الباحثين سيقيمون أيضًا تطور الداء. ويقول: “يجب أن تحدث فرقًا كبيرًا…لا يوجد سبب [لإجراء] جراحة باضعة لتحقيق تحسن طفيف”.
والباحثون يخططون لاستخدام طرق التصوير الشائعة لتحديد عدد الخلايا المنتجة للدوبامين في المرضى. لكنه قد يكون من الصعب اكتشاف التأثير الوقائي. ويقول سولزر: “المشكلة الرئيسة في جميع تجارب الحماية العصبية في داء باركنسون هي أن التشخيص يبدأ بعد موت أكثر من 50% من الخلايا المنتجة للدوبامين”. فإذا لم يكن التحسن كبيرًا، “فستكون الإشارة أصغر من أن تُكتشف”.
والفريق سيبحث أيضًا عن الفوائد الإكلينيكية (السريرية). ولكن نظرًا لأن الباحثين يقيّمون أعراض داء باركنسون من خلال مراقبة المرضى الذين يؤدون مهامّ محددة، فإن التقييمات ذاتية إلى حد كبير، وتتباين الأعراض بمرور الوقت؛ يقول سولزر إن كل شخص لديه أيام جيدة وأيام سيئة. ونظرًا لأن المجموعة الضابطة (التحكم) Control group لن تخضع لعملية جراحية، فسيكون من الصعب جدا استبعاد تأثيرات العلاج الغفل.
ومع ذلك، يمنح سولزر الدراسات مثل دراسات ابن عبيد فرصة. ويقول إن عدم وجود آلية واضحة ليس سببا لرفض العلاج. ويقول سولزر: “هناك أشياء كثيرة لا نفهمها….أنا متشكك، حتى وإن كنت أعتقد أيضًا، أن هذا مجال مثير يستحق أن نبحث فيه”.
نبذة عن الكاتبة:
جنجان سينها Gunjan Sinha، صحافية علمية تقيم في برلين.
© 2020, American Association for the Advancement of Science. All rights reserved





