أوبئة التهاب السحايا المخية النخاعية (الشوكية)
أوبئة التهاب السحايا المخية النخاعية (الشوكية)
ما زال التهاب السحايا meningitis، وهو مرض موهن وفي أغلب
الأحيان مميت، منتشرا في كثير من البلدان النامية. وقد تساعدنا
التبصرات الحديثة على توقع حدوث جائحات هذا المرض والسيطرة عليها.
<S.P.مور> ـ <V.C.بروم>
بحلول منتصف الشهر 4/1988، كان وباء التهابا السحايا في نجامينا (عاصمة تشاد) قد بلغ مداه. وقد بدأت الجائحة بعدد قليل من الحالات المنفردة في منتصف الشهر 2/1988؛ وفي غضون أربعة أسابيع كان يتم حجز نحو 150 مريضا يوميا في مشفى (مستشفى) المدينة المركزي. وعندما تم شغل جميع أسرّة المشفى كان المرضى يعالَجون في خيام عسكرية ضخمة متناثرة في كل مكان من الأفنية الداخلية للمشفى. وعلى الرغم من جهود وزارة الصحة المحلية والهيئات التطوعية الأجنبية، فقد استمر الوباء في الانتشار. وقد زاد نقص الأدوية من أعباء العاملين في القطاع الصحي، الذين عانوا إرهاق العمل أيامًا طويلة. وعلى الرغم من تنفيذ برنامج ضخم للتلقيح vaccination قد يؤدي إلى القضاء على الوباء في النهاية، فإن كل يوم كان يهدد بتفاقم الشلل الذي أصاب جهاز الرعاية الصحية الهش في تشاد.
ومع انتهاء الكارثة، كان هناك نحو 4500 شخص قد أصيبوا بالتهاب السحايا، حسب الإحصاءات الرسمية. غير أن هناك المئات ـ وربما الآلاف ـ الذين لم يشملهم الإحصاء. وفي تشاد، كما في كثير من الأقطار الإفريقية، لا تتوافر الرعاية الصحية عموما لأولئك الذين يقطنون خارج المدن الكبرى. لذا فإن المصابين بالتهاب السحايا الذين يسكنون مناطق تبعد أكثر من مسيرة يوم عن أقرب مركز صحي، لا يتلقون علاجا بالصادات (المضادات الحيوية) على وجه العموم. مما يؤدي إلى وفاة العديد منهم أو إصابتهم بتلف دماغي دائم.
 |
| مريض بالتهاب السحايا يقبع مع والده في مشفى (مستشفى) إفريقي. ويمكن أن يؤدي العلاج بالصادات (المضادات الحيوية) إلى تقليل نسبة الوفيات بسبب هذا المرض إلى 10 في المئة. لكن أغلب الأشخاص الذين يصابون بهذا المرض يعيشون في المناطق الريفية من الأقطار النامية ولا يستطيعون عموما، الوصول إلى خدمات الرعاية الصحية أو إلى المشافي مثل هذا المريض. |
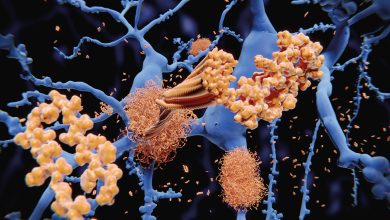
ويميز الاضطراب والبؤس اللذان سببهما الوباء في تشاد معظم جائحات التهاب السحايا بالمكورات السحائية meningococci، المعروف باسم التهاب السحايا النخاعية (الشوكية) spinal meningitis. والسمة المميزة للمرض هي بدايته الفائقة السرعة، التي أكسبت هذا المرض درجة غير عادية من «الاهتمام» وسط الخبراء الطبيين. ويصاب الشخص السليم أولا بحمى وفتور (دعث)malaise مشابهين لما يحدث عند الإصابة بالإنفلونزا (النزلة الوافدة). لكن هذه الأعراض ما تلبث أن تتحول، خلال ساعات قليلة، إلى صداع شديد وتيبّسrigidity في الرقبة ونُفور من الأضواء الساطعة. وإذا لم تتم المعالجة فقد يصاب المريض بالغيبوبة (السُّبات) coma ويتعرض في النهاية لنوع مميت من الصدمةshock. وعلى الرغم من ندرتها في الولايات المتحدة حاليا، فإن الأوبئة الشديدة مازالت تصيب أغلب دول العالم النامي؛ فقد يصاب جميع سكان قُطْرٍ ما خلال أسابيع معدودة.
لماذا تحدث كل هذه الأوبئة؟ وما الذي يدفع مرضا مثل التهاب السحايا لأن يجيش وسط مجموعة سكانية سنين عدة ثم يتفجر فجأة؟ ومع أن كثيرا من الغموض مازال يحيط بهذا المرض الفتاك، فإن وبائياته epidemiology المميزة تقدم لنا بعض الأدلة عن أسباب التهاب السحايا وكيفية الوقاية منه. فهذا المرض يتضمن دورات من الإصابة قد تكون مقابلة للتغيرات البيئية وللأنماط المناعية الشاذة، إضافة إلى ارتباطه بغيره من الأمراض الخمجية (المُعْدية). وقد بدأت الأبحاث الطبية والتقنيات البيولوجية الحديثة بكشف النقاب عن بعض هذه الأسرار المميتة.
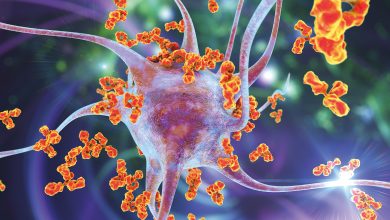
والبكتيريا (الجراثيم) المسببة لالتهاب السحايا بالمكورات السحائية، أو المسماة بالنيسرية السحائية (نيسريا منينجتيدس) Neisseria meningitidis، قريبة الصلة بالبكتيريا المسببة لمرض السَّيَلان البُنّيّ gonorrhea. لكن المكورة السحائية، وبعكس بكتيرة السيلان البني، كثيرا ما تستوطن بطانة الحَلْق ومن ثم تنتشر بسهولة خلال الإفرازات التنفسية. وهذه البكتيريا واسعة الانتشار لدرجة أنه يمكن جدلا، اعتبارها، جزءًا من النبيت الطبيعي (الفلورا) flora في الفم البشري ـ ففي أي لحظة، يحمل من 2 إلى 10 في المئة من الأشخاص الأصحاء بكتيرة المكورة السحائية. وفي جميع الاحتمالات حمل معظمنا البكتيرة في وقت ما من حياته.
وتعمل البطانة الظهارية (الطلائية) epithelial lining للحلق، عادة، حاجزا يمنع مرور البكتيريا، لكن التوازن بين الاستيطان والغزو البكتيري يختل أحيانا مما ينتج منه مرض فتاك يهدد الحياة. ويبدأ التهاب السحايا بالمكورات السحائية عندما تغزو البكتيرة مجرى الدم وتخترق السحايا ـ وهي الأغشية المحيطة بالدماغ والحبل (النخاع) الشوكي ـ لتصل إلى السائل المخي النخاعي (الشوكي) (cerebrospinal fluid (CSF الذي يغمر الجهاز العصبي المركزي (CNS). ويعمل هذا السائل كمستَنْبَت للنمو السريع للبكتيريا، مما يسبب التهاب البطانة السحائية.
وتنتج الأعراض النمطية للمرض ـ التي تشمل الحمى ويبوسة الرقبة والصداع والغيبوبة ـ من الالتهاب inflammation. وتحدث صدمة إنتانية septicshock شديدة في نحو 30 في المئة من المرضى بسبب انتشار المكورات السحائية في كل مكان من الجهاز الدوري. وتتسم هذه الصدمة بهبوط شديد في ضغط الدم، لا سيما في الأطراف. ويحتمل أن يكون هذا التفاعل ناتجا من انطلاق ذيفانات داخلية endotoxins من البكتيرة مما يحفز إنتاج بعض البروتينات، مثل عامل نخر الورم tumor necrosis factor a. وتزيد هذه العوامل، بدورها، من نفاذية الأوعية الدموية. ويمكن أن يتسبب مثل هذا التغير في حدوث هبوط مميت في ضغط الدم. ويمكن للمرضى الناجين من الموت بفعل الصدمة الإنتانية الناتجة من المكورات السحائية أن يعانوا التشوّه المتمثل في فَقْد الجلد وأجزاء من الأطراف. والالتهاب السحائي مرض مميت لو لم تتم معالجته؛ إذ يقلل التدخل السريع بالصادات من معدل الوفيات إلى نحو 10 في المئة. وقد يعاني الناجون اضطرابات عصبية مثل الصمم والشلل والتخلف الذهني (العقلي).
لم تحدث أوبئة من التهاب السحايا في الولايات المتحدة أو أغلب الدول الصناعية الأخرى منذ الحرب العالمية الثانية. وعلى الرغم من انتشار حَمْلcarrying البكتيرة، فإن عدد الإصابات بالتهاب السحايا بالمكورات السحائية المتوطن endemic يقل عن ثلاث حالات لكل 000 100 من السكان في الولايات المتحدة سنويا. ومع هذا فمازالت الأوبئة المفوَّعة virulent على وجه الخصوص، تصيب الأقطار النامية. فقد تم تسجيل أكثر من 000 400 إصابة مرضية في إثيوبيا خلال وباء العام 1989، في حين بلغت حالات الإصابة في الصين نحو ثلاثة ملايين خلال الستينات. وقد يحمِّل التدفقُ المفاجئ لمئات أو آلاف الحالات المرضية أجهزةَ الرعاية الصحية في الأقطار النامية ما هو فوق طاقاتها، التي كثيرا ما تكون بدائية.
وتعدّ دراسة العملية الوبائية ذاتها أمرا صعبا نظرا لأن الجائحات المرضية عادة ما تكون غير متوقعة وغير متكررة الحدوث. ويكوّن شريط عريض من الأقطار الإفريقية الواقعة في جنوب الصحراء الكبرى ما يسمى «بحزام التهاب السحايا»، وتتكون هذه المنطقة من سهول الساڤانا العريضة، المعشوشبة، الممتدة من غامبيا في غرب إفريقيا عبر القارة وصولا إلى إثيوبيا. وقد عرف علماء الوبئيات، منذ عقود عدة، أن الأوبئة عالية الانتشار في هذه المنطقة على وجه الخصوص وأنها تميل للتكرر كل خمسة إلى اثني عشر عاما. وتستغرق كل من الموجات الوبائية عدة سنوات.
وتتبع معدلات التهاب السحايا في أي سنة بعينها دورة سنوية ثانية: يبلغ عدد هذه الإصابات المرضية أقصاه خلال موسم الجفاف ويتلاشى مع بداية الأمطار. وحتى خلال ذروة انتشار الوباء يقل معدل الإصابات المرضية ليصل إلى مستوى خط القاعدة baseline خلال موسم الأمطار، ويعود للارتفاع ثانية مع حلول موسم الجفاف التالي. لهذا، يبدو أنه عند سريان بكتيرة المرض بين أفراد مجموعة سكانية عرضة للإصابة، فهناك حدثٌ ما ـ خلال موسم الجفاف ـ سيحدِّد إن كان الوباء سيصيب هذه المجموعة أو لا.
 |
| يقطع حزام التهاب السحايا وسط إفريقيا، من إريتريا شرقا إلى غامبيا غربا. ويبدو أن سكان هذه المناطق معرّضون بصورة فريدة، لأوبئة التهاب السحايا المتكررة. وتنتج الجائحات في هذا الحزام في أغلب الأحيان من الخمج بسلالة واحدة ومحددة من البكتيريا، وهي المجموعة المصلية A من المكورات السحائية. |
وقد حيّرت هذه السمات الغامضة لكوارث المكورات السحائية علماء الوبئيات لسنوات. فعوامل الخطر المتعلقة بوباء، بعكس تلك المتعلقة بالأمراض المتوطنة، قد تصيب شعبا بأسره وليس مجموعات متناثرة من الأفراد فحسب. ولأن احتمال حدوث الأوبئة يختلف بمرور الزمن، فيجب بالمثل أن تتفاوت العوامل المسؤولة عن بدايته. ففي الولايات المتحدة على سبيل المثال، يكون الأفراد المولودون بنقص وراثي نادر في الجهاز المتمم (الجملة المتممة) complementsystem (وهو سلسلة من بروتينات الدم التي يتم تنشيطها بفعل الأضداد (الأجسام المضادة) antibodies لقتل البكتيريا) معرَّضين بصورة غير عادية للإصابة بالتهاب السحايا بالمكورات السحائية. ولأن المرض ذاته نادر في أمريكا، فقد تنتج نسبة كبيرة من الإصابات المرضية من هذا النقص الوراثي. ومع هذا، يبدو أن عدد الأفراد المعرضين لهذه الإصابة يميل إلى الثبات، لذلك فمن غير المحتمل أن يكون هذا النقص الوراثي سببا مهما لحدوث وباء مرضي. وفي الواقع، إن الدراسات ـ التي أجريت في نيجيريا وغامبيا ـ قد أثبتت أن المرضى المصابين بعوز في الجهاز المتمم لا يشاهَدون عادة خلال هذه الجائحات.
وبعكس العوز في الجهاز المتمم، فإن عوامل أخرى في العائل (الثويّ) host ـ مثل معدلات الأضداد للمكورات السحائية ـ قد تتغير في مجموعة سكانية ما بمرور الزمن. ويعرف المعدل العام لمناعة مجموعة سكانية ضد كائن organismمعين باسم مناعة القطيع herd immunity، وهو مصطلح يعود إلى بدايات الدراسات المناعية التي أجريت على الماشية. ويمكن أن يكون انخفاض مناعة القطيع لمجموعة سكانية مسؤولا بصورة جزئية عن الأنماط الدورية لالتهاب السحايا في إفريقيا.
وفي أواخر الستينات، أجرى <I. گولدشنيدر> و <E .C. گوتشليش> وزملاؤهما (من معهد وولتر ريد العسكري للأبحاث) دراسات ممتازة أظهرت أهمية دفاعات العائل في مواجهة المكورات السحائية. فقد كان المجندون في الجيش ـ قبل ظهور التلقيح ضد المرض في السبعينات ـ معرّضين بدرجة كبيرة للإصابة بالتهاب السحايا. وقد قامت مجموعة معهد وولتر ريد بسحب عينات من دماء آلاف المجندين عند بداية تدريبهم العسكري الأساسي ثم متابعتهم خلال فترة معسكر التدريب. وعند إصابة أحدهم بالمرض كانت تختبر قدرة مصل (سيروم) دمه المحفوظ على قتل المكورات السحائية، ثم تتم مقارنتها بالنشاط المضاد للمكورات السحائية في مصل دماء أقرانه الأصحاء.
كيف تهاجم المكورات السحائية الجسم؟
|
وقد وجد الباحثون أن المرض يحدث أساسا لدى المجندين الذين تتسم أمصال دمائهم بنشاط ضعيف لمقاومة المكورات السحائية قبل إصابتهم بالمرض. وقد بَدَت هذه النتائج غير معقولة، نظرا لأن أغلب البالغين لديهم أضداد وقائية ضد المكورات السحائية. ومن الواضح أنه على المرء أن يتعرض للإصابة بالكائن لكي يكتسب لها أضدادا. ومع هذا فقد أثبتت الدراسات، التي أجريت على المجندين، أن الأفراد الذين لا يملكون أضدادًا يكونون أكثر عرضة للمرض عند تعرضهم للمكورة السحائية. ولم يكن من الواضح سبب اكتساب أغلب الناس للأضداد الوقائية عند تعرضهم للمكورة السحائية أول مرة بدلا من إصابتهم بالمرض.
وقد تتمثل الإجابة عن هذا التناقض الظاهري في البكتيريا غير المُمْرِضَة التي تكوّن جزءا من النبيت الفموي الطبيعي للإنسان، ومنها النيسرية اللبنية (نيسريا لاكتاميكا) Neisseria lactamica، وهي قريبة الشبه بالنيسرية السحائية (نيسريا مننجتيدس). وقد أوضح كل من <R. گولد> و<L .M. ليبو> (من جامعة كونكتيكت)، بالاشتراك مع باحثي معهد وولتر ريد، أن الأطفال الذين يصابون بأخماج الحلق بالنيسرية اللبنية كثيرا ما يكتسبون أضدادا تقيهم أيضا من الإصابة بالمكورات السحائية. وعلى هذا فيبدو أن الخمج بأحد أنواع البكتيريا غير المُمْرِضَة يمنح الجسم مناعة ضد الإصابة بسلالات (ذرارٍ) strains أخرى أكثر فوعة. وهذا النمط يقدم لنا تفسيرا للتجربة مع المجندين، أي أن كل مجند لا يمتلك جسمه أضدادًا تبادلية الوقاية cross-protective ـ كنتيجة لإصابته في مرحلة الطفولة بالخمج بإحدى سلالات النيسرية ـ يكون معرضا بصورة خاصة للإصابة بالمرض لأن سلالات المكورة السحائية من جميع أرجاء القطر تنتشر بسرعة بين رفاق الثكنات العسكرية.
ومازالت الأبحاث تحاول تحديد أيٍّ من مكونات المكورة السحائية يسبب الاستجابة (ردة الفعل) المناعية الواقية من الإصابة بالمرض. وللمكورة السحائية مستضدات (مولدات الضد) antigens (وهي جزيئات تثير الاستجابات المناعية)، وأحدُ هذه المستضدات المِحْفظةُ عديدة السكريدات polysaccharide capsule التي تحيط بالبكتيرة. وتمتلك سلالات المكورة السحائية مستضدات عديدة السكريدات مختلفة، وقد تم تحديد 13 نوعا على الأقل من عديدات السكريدات سميت بالمجموعات المصلية serogroups. وتتسبب المجموعة المصلية A للنيسرية السحائية في حدوث الأوبئة الكبرى التي تجتاح كلاً من إفريقيا والصين وأمريكا الجنوبية من وقت لآخر.
أما المجموعات المصلية الأخرى فهي أقل احتمالا في إحداث الأوبئة، على الرغم من أنها تسبب أغلب الحالات المرضية المتوطنة في الولايات المتحدة. وتُعَدّ اللقاحات المحضرة من نوع ما من عديدات السكريدات فعالة للغاية ضد المجموعات المصلية المقابلة، إلا أنها لا توفر حماية متبادلة. ولسوء الحظ فإن عديدات السكريدات للمجموعة المصلية B، وهي أكثر المجموعات المصلية شيوعا في الولايات المتحدة، لا تثير حدوث استجابة مناعية دائمة.

|
| يتبع المعدل السنوي للإصابة بالتهاب السحايا في <بوركينا فاسو> نمطا مثاليا لأقطار حزام التهاب السحايا. فالأوبئة تنحو للاستمرار عدة سنوات وتتبع نمطا تصاعديا-تنازليا (في الأعلى). لكن هذه المعدلات شديدة الموسمية، حتى أثناء انتشار الوباء، وكما يبدو من الرسم التوضيحي (في اليمين)، فالجائحات تحدث فقط أثناء موسم الجفاف الذي يبدأ من الشهر 1 ويستمر حتى الشهر 6. |
وتشير الأبحاث التي أجراها <M .J. گريفيس> و <E .R. ماندريل> وغيرهما (في جامعة كاليفورنيا بسان فرانسيسكو) إضافة إلى <D .W. زولنگر> ومجموعته (في معهد وولتر ريد) إلى مستضدات ـ إضافة إلى عديدات السكريدات ـ تلعب أيضا دورا مناعيا مهما ضد المرض. ولأن الوقاية ضد عديدات السكريدات ليست وقاية متبادلة، فمن المحتمل أن المناعة الواسعة التي توفرها الإصابة بالنيسرية اللبنية إنما تحدث بفعل مستضدات أخرى. وفي الواقع، إنه من المحتمل ألا تمتلك النيسرية اللبنية محفظة عديدة السكريدات على الإطلاق. وقد تكون المناعة ناتجة بفعل مكوِّنات خلوية أخرى ـ مثل بروتينات الغشاء الخارجي والليپيدات قليلة السكريدات lipooligosaccharides المرتبطة بالغشاء الخلوي والموجودة في كل من النيسرية السحائية والنيسرية اللبنية.
وقد تفسر لنا هذه الآلية المناعية سبب حدوث أوبئة التهاب السحايا في إفريقيا في فترات تفصل بينها مدد زمنية تتراوح بين 5 و12 سنة. فالمعدلات المرتفعة من الخمج بالمكورات السحائية خلال فترة انتشار الوباء قد تتسبب في حدوث مناعة طبيعية واسعة النطاق تقي السكان لاحقا من الإصابة بالمرض لسنوات عديدة. ومع تناقص هذه المناعة نتيجة ولادة أطفال معرضين للإصابة، وبفعل الفَقْد الطبيعي للأضداد يصبح السكان معرضين لوباء جديد.
ومع ذلك، لا يقدم فقد المناعة تفسيرا كاملا للأنماط الخادعة التي يتخذها المرض في أقطار حزام التهاب السحايا، فموسمية المرض توضح أن للعوامل البيئية أهميتها المحورية. ونحن ندين بأغلب ما نعرفه عن هذه العوامل البيئية للدراسات التي أجراها في غامبيا ونيجيريا فريق من الباحثين بقيادة <M .B. گرينوود> من مخابر (مختبرات) مجلس الأبحاث الطبية في المملكة المتحدة، فقد انهمكت هذه المجموعة بنشاط في الكشف عن وبئيات هذا المرض، إضافة إلى قيامها بتصميم البرامج الجديدة للتلقيح والسيطرة على هذا المرض. وقد وجد گرينوود وزملاؤه أن انتقال المكورات السحائية يحدث طوال العام، على الرغم من أن المرض ذاته لا يظهر إلا خلال موسم الجفاف.
إضافة إلى هذا، يمكن اكتشاف معدلات مرتفعة من الأضداد في بعض القرى بعد انتهاء موسم الأمطار (الذي لا تحدث خلاله أي إصابات مرضية)، مما يشير إلى انتشار المكورات السحائية بين سكانها، وبالتالي يزيد من مناعتهم دون الإصابة بالمرض، لذا فإن موسمية التهاب السحايا في إفريقيا لا تنتج من زيادة في انتقال البكتيرة خلال موسم الجفاف. ويبدو في المقابل أن درجات الحرارة المرتفعة والرطوبة المنخفضة يجعلان الأفراد أكثر عرضة للمرض بمجرد إصابتهم بالبكتيرة. وقد يزيد جفاف البطانة المخاطية mucosal lining للحلق خلال موسم الجفاف من استعمار colonization المكورات السحائية للأنسجة الواقعة تحتها.
إضافة إلى العوامل المناخية، فإن الأخماج الڤيروسية viral للمسلك التنفسي العلوي قد تصيب الأغشية المخاطية البلعومية بالمثل، مما يجعلها أكثر عرضة للإصابة بالغزو البكتيري. ويمكن أن يحدث التهاب الرئة (ذات الرئة) pneumoinaالبكتيري، على سبيل المثال، في أعقاب الإصابة بالأخماج الڤيروسية. وقد أصبحت مجموعتنا في فرع التهاب السحايا والمُمْرِضات الخاصة في مراكز الوقاية من الأمراض ومكافحتها (CDC) مهتمة بهذا الاحتمال خلال سلسلة من الأوبئة التي ظهرت في أواسط الثمانينات.
وفي الشهر 8/1987، اتصلت بنا سلطات الصحة العامة في مدينة نيويورك وأخبرتنا بأن هناك شخصين قد أصيبا بالتهاب السحايا خلال رحلتين جويتين منفصلتين قادمتين من المملكة العربية السعودية. وكانت المراكز CDC قد تلقت في الأسبوع السابق تقارير تفيد بأن التهاب السحايا بالمكورات السحائية آخذ في التفشي بين المشاركين في رحلة الحج السنوية للمسلمين إلى مكة المكرمة، لكنه لم يكن من الواضح أن هناك وباء في طريقه إلى الحدوث (وقد نتج من الوباء الذي أصاب مكة المكرمة في العام 1987 ما لا يقل عن 000 10إصابة بالتهاب السحايا). وعليه فقد غادر كل من <H .L. هاريسون> (وهو عالم آخر بالوبئيات) و<W .G. آگيلّو> (وهي عالمة بالأحياء المجهرية) وأحد المؤلّفيْن (مور) إلى مطار <F.J. كندي> الدولي لمقابلة ركاب الطائرات القادمة والناقلة للحجّاج.
 |
| يمكن استخدام الرحلان الكهربي الإنزيمي enzyme electrophoresis لاكتشاف التباعد divergence بين سلالات البكتيريا، فتوضع الإنزيمات داخل الخلوية من سلالات متعددة في هلامة حيث تنفصل عند إمرار تيار كهربي في المزيج، ويتم تعرّف كل إنزيم عن طريق طفراته الفردية ـ التي تميز تباعده عن غيره. وتنتقل إنزيمات السلالات المختلفة إلى أماكن متفرقة من الهلامة. ويمكن بهذه الطريقة اختبار إنزيمات عديدة لتحديد تماثلها من عدمه. |
 |
| كان يُعتقد أن المجموعة المصلية A من المكورات السحائية متجانسة، لكن دراسات الرحلان الإنزيمي أظهرت أن المجموعة المصلية A من المكورات السحائية تتكون على الأقل من 21 من السلائل lineages أو النسائل clones. ومؤخرا، تسببت إحدى هذه النسائل، وهي النسيلة III-1، في إحداث الأوبئة في آسيا والشرق الأوسط وإفريقيا. |
وقد قمنا بإعداد مستوصف عند طابور التجمع في باحة المطار لتقديم الصادات الوقائية. ومن بين المسافرين الذين تم فحصهم والبالغ عددهم 550، وجدنا أن 11 في المئة من القادمين من مكة المكرمة كانوا حاملين للمجموعة المصلية A من المكورات السحائية ـ وهي سلالة شديدة الندرة في الولايات المتحدة. وقد وُجِد أن الأفراد الحاملين للبكتيرة هم عرضة للإصابة بأعراض الزكام، مثل ارتفاع درجة الحرارة والتهاب الحلق، أكثر من غير الحاملين لها. لكن هذا الدليل كان ظرفيا فحسب، نظرا لأننا قد قمنا بفحص الحاملين للمكورة السحائية وحدهم، وليس المصابين بالتهاب السحايا. لذا فقد كانت الخطوة التالية هي البحث المباشر عن أخماج المسلك التنفسي العلوي لدى أولئك المصابين بالتهاب السحايا بالمكورات السحائية.
وقد أتيحت لنا هذه الفرصة خلال انتشار الوباء الذي اجتاح تشاد. ففي صبيحة أحد الأيام من الشهر 4/1988 تلقينا اتصالا هاتفيا من <T. ليبڤيلد> (من معهد هارڤارد للتنمية الدولية) مفاده أن نجامينا، وهي مدينة يقطنها نحو 000 500 نسمة وتقع في قلب حزام التهاب السحايا، تعاني أحد الأوبئة الكبرى بفعل المجموعة المصلية A من المكورات السحائية. وقد كانت وزارة الصحة المحلية، برئاسة <M .P.يانكالبيه>، تقوم بتنظيم جهود المكافحة بالتعاون مع مجموعة بيوفورس الفرنسية ـ وهي مجموعة من أطباء الصحة العامة أنشأتها وزارة الصحة الفرنسية ـ ومعهد ميرييه في مدينة مرسيليا. وقد حصلنا على موافقة الحكومة التشادية لإجراء استقصاء، وعليه فقد سافر فريق من المراكز CDC إلى نجامينا لإجراء دراسة مشتركة مع أطباء المشفى المركزي هناك.
ومن أجل البحث عن الأخماج التنفسية، فقد قمنا بإجراء مقابلة (مناظرة)matching دقيقة بين الأفراد المصابين بالتهاب السحايا وبين مجموعة ضابطةcontrol group تتكون من أشخاص أصحاء من نفس العمر والجنس والجوار. وقد تم تجميع عينات من الغسولات الأنفية ثم أُرسلت إلى <J. هيرهولتزر> في المراكز CDC، الذي اضطلع بالمهمة الشاقة لإعداد واستزراع (استنبات) culturing مئات من الغسولات الأنفية. وقد كانت النتائج مدهشة، فقد كان مرضى التهاب السحايا على وجه العموم ـ معرّضين لحمل العوامل المُمْرِضَة pathogens في المسلك التنفسي العلوي بنسبة تزيد على نسبة المجموعة الضابطة بثلاثة وعشرين ضعفا. ولم يكن أولئك المرضى معرّضين للإصابة بمثل هذه الڤيروسات فحسب، لكن نسبة كبيرة منهم كانت مصابة ببكتيرة داخلوية (داخل خلوية) تسمى «بالمتفطرة البشرية» (ميكوبلازما هومينيس) Mycoplasma hominis.
وتقترح هذه النتائج وجود سبب آخر لموسمية أوبئة التهاب السحايا. وربما كان مزيجا من الرطوبة المنخفضة والأخماج التنفسية هو ما يجعل السكان عرضة للإصابة بالمرض. ونحن بحاجة إلى المزيد من الأبحاث لتوضيح الآلية التي تتفاعل (تتآثر) interact بها الأخماج التنفسية مع المكورة السحائية. وعلى الرغم من ذلك، فإن <S .D. سيتفنس> (من جامعة إيموري) و<A .Z. ماك جي> (من جامعة يوتا) قد أوضحا مخبريا أن خلايا البطانة البلعومية يمكنها، تحت ظروف معينة، أن تمتص المكورات السحائية، كما يمكن أن تثير الأخماج التنفسية عملية الامتصاص (القَبْط) uptake هذه بطريقة يمكن تخيلها. وعلى العكس من ذلك، يمكن للأخماج التنفسية أن تتلف الأغشية المخاطية مباشرة، أو أن تثبط الخلايا المناعية الموجودة فيها.
وقد ارتبطت الأخماج التنفسية بمرض المكورات السحائية (التهاب السحايا) في الأقطار الصناعية كذلك، تمشيا مع حقيقة أن تفشي المرض يزداد خلال أشهر منتصف الشتاء، مع انتشار ڤيروسات الزكام. وقد لاحظ مؤخرا كل من <A .K. كارترايت> و<M .D. جونز> و <M .J. ستيوارت> وزملائهم (من قسم الصحة العامة في گلوسيستر بإنكلترا) وجود ارتباط مماثل بين الخمج بالمكورات السحائية والخمج بڤيروس الإنفلونزا (النزلة الوافدة). وقد اكتَشف وجود العلاقة نفسها <B. هوبير> وزملاؤه في الإدارة العامة للشؤون الصحية في فرنسا. وقد يؤدي هذا البحث لاكتشاف طرق جديدة لتوقع حدوث الأوبئة في هذه الأقطار. ومن المثير للسخرية أن أسبابَ موسميةِ أخماج المسلك التنفسي العلوي مازالت بهذا الغموض.
 |
| حديثا، تسببت البكتيرة الرحالة، أي النسيلة III-1 من المجموعة المصلية A من المكورات السحائية، في انتشار وباء على نطاق عالمي. وتشير أنماط وتواقيت حدوث هذه الأوبئة إلى أن المسافرين قد حملوا الخمج معهم من آسيا ـ حيث موطنه الأصلي ـ إلى مكة المكرمة ومنها إلى سائر أقطار «حزام التهاب السحايا» بما فيها إثيوبيا وكينيا. |
وأثناء قيامنا بالبحث في تشاد، تمكنت وزارة الصحة هناك من السيطرة على الوباء، الذي تم القضاء عليه في النهاية نتيجة لتضافر جهود مجموعة هارڤارد وأطباء المشفى المركزي والمتطوعين الأجانب. وقد قدمت الكثير من الحكومات، ومنها حكومتا الولايات المتحدة وفرنسا، العون لتشاد أثناء انتشار الوباء. وقد أصيب بالتهاب السحايا نحو واحد في المئة من كل سكان نجامينا (بلغت نسبة الإصابة في بعض المجموعات السكانية مثل أطفال المدارس والجنود نحو 10 في المئة). وربما بلغت الإصابة معدلات أعلى لو لم يتم اتخاذ الإجراءات المناسبة للسيطرة على الوباء. وقد كان هذا من الأمثلة الواضحة على التحرك الدولي المطلوب عند حدوث مثل هذه الأوبئة.
وإذا ما كانت الأضداد والعوامل المناخية والأخماج لازمة لتشكل الوباء، فما الدور الذي تلعبه البكتيرة ذاتها؟ يمكن أن يساعدنا في الإجابة عن هذا السؤال التخصص الحديث بالوبئيات الجزيئية molecular epidemiology، إذ يمكن لعلماء الوبئيات حاليا، باستعارة بعض من تقانات علم البيولوجيا الجزيئية مثل سَلْسَلَة الدنا sequencing DNA والرَّحَلان (التهجير) الكهربي الإنزيمي enzyme electrophoresis، أن يحلوا غموض الجائحات التي تتسبب في حدوثها ذرية سلالة منفردة أو نسيلة clone واحدة من البكتيريا. وقد استطاعت هذه التقانات بالفعل أن تقتفي أثر عدد من المُمْرِضات البكتيرية والڤيروسية، وقد أثبتت فاعليتها على وجه الخصوص في اكتشاف حالة لانتقال ڤيروس العوز المناعي البشري (HIV) من طبيب أسنان في فلوريدا إلى عدد كبير من مرضاه.
ومثلما يمكن للبيولوجيين أن يستخدموا عملية تراكم الطفرات mutations ـ التي تحدث مع مرور الزمن ـ لتعقب التباعد divergence التطوري بين نوعيْنspecies من الأحياء، يستطيع علماء الوبئيات بالمثل تحليل الدنا، بحثا عن الطفرات التي تمكّنهم من التفريق بين سلالتين لنفس الكائن الحي المجهري أثناء سريانهما عبر المجموعات السكانية البشرية. وقد تم التوسع في استخدام طريقة غير مباشرة لفحص القرابة الوراثية بين السلالات المختلفة تسمى بالرحلان الكهربي الإنزيمي عديد المواقع، لتعقب المجموعة المصلية A من المكورات السحائية.
ويعتمد هذا التطبيق البسيط بَدْهِيًّا والقوي في الوقت نفسه، على اكتشاف الطفرات التي تغير من تَسَلْسُل الأحماض الأمينية للإنزيمات البكتيرية. ولا تؤثر هذه الطفرات عموما في النشاط الكيميائي للإنزيمات، لأنها لو فعلت ذلك لتعرضت السلالة البكتيرية للفناء. ومع ذلك، فقد تتسبب الطفرات الصغرى بدمج الأحماض الأمينية المختلفة الشحنة الكهربية في الإنزيم، الذي يمكن الكشف عنه بعد ذلك بوساطة الرحلان الكهربي. فإذا ما وضعت هيولى (سيتوبلازم) cytoplasm سلالتين بكتيريتين مختلفتين في هلامة gel ثم مرِّر تيار كهربي، سترتحل (تهاجر) الإنزيمات عبر الهلامة ـ بسرعات متباينة ـ إذا كان هناك اختلاف في تسلسل الأحماض الأمينية في كل منهما.
وإذا ما تباعدت، حديثا، سلالتان من المجموعة المصلية A للمكورات السحائية إحداهما عن الأخرى، سيكون هناك احتمال ضئيل لتراكم الطفرات في أي إنزيم بعينه. وعليه ستكون مقارنة الرحلان الكهربي للسلالتين متشابهة. وكلما زادت درجة الاختلاف بين السلالتين، زاد عدد الإنزيمات المختلفة بينهما في الرحلان الكهربي. ويمكن مقارنة إنزيمات عدد من السلالات باستخدام تقانة إحصائية تسمى التحليل العنقودي (الجماعي) cluster analysis. ويمكن أن تكشف هذه العملية الاختلاف الوراثي النسبي بين السلالات المختلفة. فكل مجموعة من السلالات المتشابهة تمثل نسيلة مستقلة تتقارب فيها جميع المعزولات isolates المفردة لدرجة كبيرة، وربما كانت مستمدة من خلية سَلَفِيّة (سليفة) ancestral حديثة واحدة. ويمكن للباحثين دراسة هذه السلالات، ومن ثم تكوين شجرة عائلية family tree لكل من النسائل المختلفة.
وفي برنامج طموح، استخدم <M. آختمان> و<T. أوليهوك> و<A .B. كراو> (من معهد ماكس بلانك للوراثة الجزيئية في برلين) هذه التقانة لدراسة 423 من سلالات المجموعة المصلية A من المكورات السحائية. وقد أتاحت لهم تحليلاتهم هذه تحديد وراثة العشائر (الوراثيات السكانية) population genetics لهذه المجموعة المصلية: يمكن تقسيم السلالات إلى أربع زمر جزئية (مجموعات فرعية)، يمكن أن تنقسم بدورها إلى ما مجموعه إحدى وعشرون نسيلة مختلفة. وعلى الرغم من أن شجرة العائلة هذه هي أبعد ما تكون عن الاكتمال (لم يتم حفظ الكثير من السلالات التي تسببت في حدوث جائحات وبائية في الأقطار النامية، كما تم اكتشاف وجود زمرة جزئية خامسة) فإنها تقدم لنا إطارا لمقارنة الكمونات الوبائية للسلالات المختلفة.
ومن المعقول أن نفترض بأن سلالات المكورة السحائية تتباعد ببطء مع مرور الزمن أثناء سريانها خلال أي مجموعة سكانية بعينها. فقد أظهرت الدراسات وجود العديد من السلالات تحت الظروف المتوطنة. وإذا ما تساوت جميع السلالات في الفَوْعَة (حِدّة الإمراض) وكانت الأوبئة ناتجة أساسا من التغيّر في عوامل كل من العائل والبيئة، ستميل الأوبئة لأن تكون عديدة النسائل لأن كل سلالة ستكون لديها فرصة متساوية للتسبب في حدوث المرض. ومع ذلك، فليس هذا هو ما يحدث في الواقع. فقد اكتشفت مجموعة برلين ـ إضافة إلى گرينوود وموسى حسن ـ كينگ في غامبيا ـ أن الأوبئة تنتج، في الغالب، بفعل نسيلة منفردة. وعلى ذلك، قد تلعب الفوعة النسيلية، دورا مهما في هذه العملية.
وبمساعدة <M. ريفز> [من قسم المخابر (المختبرات) في فرع التهاب السحايا والمُمْرِضات الخاصة] تمت دراسة السلالات المحفوظة في المراكز CDC من الأوبئة التي اجتاحت كلاً من جنوبي آسيا وإفريقيا والشرق الأوسط، بحثا عن دليل على وجود الفوعة النسيلية. وقد تم العثور بالفعل على ارتباط مدهش. فقد كان كل وباء يعد في السابق حدثا منفردا. إلا أنه، وبمجرد أن تمت مقارنة السلالات، ظهرت العلاقة بينها جلية. وقد أثبتت مجموعة آختمان سابقا أن نسيلة واحدة ـ وهي النسيلة III-1 ـ قد تسببت في حدوث الأوبئة التي اجتاحت الصين ونيپال في مطلع الثمانينات من هذا القرن. وقد أظهرت أنماط الرحلان الكهربي للسلالات المحفوظة في المراكز CDC أن هذه النسيلة نفسها قد تسببت أيضا في حدوث سلسلة من الأوبئة التي اجتاحت الصين ونيپال والسعودية وتشاد.
وقد ظهرت النسيلة III-1 أولا في الصين خلال الستينات. وقد اجتاح وباء خطير ثان وادي كاثمندو في نيبال بعد فترة وجيزة من افتتاح الطريق البري بين نيبال والتبت عام 1984. وقد انتقلت هذه السلالة إلى شمالي الهند والباكستان عام 1985 مسببة وباء آخر. ومن الواضح أنها ظلت ساكنة جنوبي آسيا حتى صيف العام 1987. فقد انتقلت النسيلة III-1 في هذا الوقت إلى مكة المكرمة عن طريق الحجاج القادمين إليها من جنوبي آسيا. وقد أثبت علماء الوبئيات من السعودية والمراكز CDC، الذين قاموا بدراسة وباء مكة المكرمة، أن هذا الوباء قد بدأ بين أولئك الحجاج الذين بلغت نسبة الإصابة فيهم أقصاها أيضا. وعندما انتهى موسم الحج، عاد حاملو النسيلة III-1 إلى أوطانهم. لذا فقد كانت عودة الحجاج الأمريكيين هي ما دفعنا لإجراء دراسة مطار كِنِدي.
 |
| تم إنشاء عيادة على وجه السرعة في مطار <F – .J. كندي> الدولي بمدينة نيويورك في الشهر 8/1987 لمعالجة المسافرين المخموجين. وقد تمت معالجة الحجاج القادمين من مكة المكرمة بالصادات، وأمكن بذلك منع حدوث وباء محتمل. |
ولسوء الحظ، فقد كان الكثير من الحجاج المسلمين القادمين من أقطار حزام التهاب السحايا حاملين للنسيلة III-1 أيضا، لذا لم يكن من المستغرب أن تظهر الجائحات في الوقت نفسه في تشاد والسودان خلال موسم الحج للعام 19888. ونتيجة لهذا، فقد انتشرت الأوبئة الناتجة من النسيلة III-1 عبر شرقي إفريقيا، مجتاحة إثيوبيا وتنزانيا وكينيا وأوغندة. ويهتم مسؤولو الصحة العامة بكمونات potentials حدوث أوبئة مماثلة في أقطار أخرى من حزام التهاب السحايا الأخرى بفعل النسيلة III-1 أيضا. وقد اجتاح وباء لالتهاب السحايا توگو عام 19933، لكنه من غير المعروف حتى الآن إن كان سبب هذا الوباء هو النسيلة III-1 ذاتها.
وعلى الرغم من أن النسيلة III-1 قد تسببت في حدوث مئات الآلاف من حالات الإصابة بالتهاب السحايا، فلا يبدو أنها مفوعة بصورة استثنائية. وبما أنه قد بات ممكنا الآن إجراء تحليل نسيلي لسلالات المكورة السحائية، فمن الواضح أن هناك نسائل أخرى قد تسببت في حدوث أوبئة مشابهة في إفريقيا وآسيا. ومع ذلك، تشير هذه النتائج إلى أن إدخال نسيلة كامنة الوبائية إلى مجتمع ما، مع توافر الظروف الملائمة لها، قد يكون فتّاكا. وقد تم طرح تفسيرين لهذه العملية: أولهما أن النسائل الوبائية تنتشر بصورة عشوائية أثناء سريانها خلال مجموعة سكانية معينة، أما الثاني فهو أنها تظل على قيد الحياة بالإفلات من مناعة القطيع. وكقياس تمثيلي لجائحات الإنفلونزا، فقد افترض أن هذه الأوبئة قد تَنتج ممّا يسمى «التحوّلات (الزيجانات) المستضدية» antigenic shifts. وعلى الرغم من اشتراك جميع سلالات المجموعة المصلية A من المكورات السحائية في نفس عديدة السكريدات، فإن النسائل المختلفة تتباين في غيرها من المستضدات المُعرَّضة exposed على السطح الخلوي. لذا، عندما تضعف المناعة ضد المستضدات المشتركة، قد تفلت نسيلة جديدة ذات مستضدات سطحية مختلفة بدرجة كافية من الترصّد (المراقبة) المناعي immune surveillance، ومن ثم تتسبب في حدوث وباء جديد. وهنا يلاحظ علماء الوبئيات المتابعين للأنماط المرضية وجود تحولات مستضدية مع حلول النسائل الجديدة محل تلك الأقدم.
وإذا ما كانت هذه التحولات المستضدية تحدث في المكورات السحائية بالفعل، فقد تنتج الدورات المرضية التي نراها في إفريقيا من مزيج من الزمن المطلوب لفقد المناعة ومتوسط الوقت الذي تستغرقه نسيلة ما للوصول إلى مجموعة سكانية معينة، وسيكون للعوامل البيئية دورها أيضا؛ لأن إدخال النسيلة وحده لا يكفي لإحداث جائحة وبائية. وإذا ما انتقل العامل المُمْرِض إلى مجموعة سكانية أثناء موسم الأمطار، فقد يتسبب هذا في تعزيز مناعة أفرادها دون إصابتهم بالمرض. وعلى الرغم من أن الظروف الدقيقة اللازمة لحدوث الوباء تظل غير معروفة على وجه التحديد، فمما يبدو أنه عند انتقال سلالة ما إلى مجموعة سكانية ذات مناعة ضعيفة أثناء موسم الجفاف، سيكون هناك خطر كبير من حدوث وباء.
وعلى هذا، يبدو أن مزيجا من عوامل كل من العائل والبيئة وتلك المتعلقة بالعامل الممرض ذاتها هي المسؤولة عن الوبئيات الفريدة لهذا المرض. وقد بدأت هذه الخصائص في التكشف مؤخرا، فمن المرجح أن الأوبئة ليست متماثلة، وأن هناك آليات أخرى مسؤولة عن بعض ـ أو كل ـ صفات جائحات التهاب السحايا. فعلى سبيل المثال، لماذا لا تتسبب السلالة III-1 في إحداث وباء في الولايات المتحدة؟ فهذه الدولة قد خلت من الجائحات الوبائية منذ الأربعينات من هذا القرن، ولذا سيبدو أن المناعة ضد السلالة III-1 ستكون منخفضة. وكما يعرف كل من أصيب بالزكام من قبل، فليس هناك بالتأكيد نقص في أخماج المسلك التنفسي العلوي في الولايات المتحدة. إضافة إلى ذلك، فلا أحد يعرف سبب نجاح الإصابة أثناء الطفولة بأخماج النيسرية في حماية سكان البلدان الصناعية وعدم وجود هذا التأثير لدى مواطني البلدان الإفريقية. ويبدو أن العوامل الاجتماعية-الاقتصادية غير المحددة جيدا هي التي تجعل البلدان الصناعية مقاومة للإصابة بالمرض. وعلى الرغم من جاذبية نظرية التحولات المستضدية، فمازالت هناك حاجة إلى إجراء دراسات طويلة المدى في إفريقيا لإثبات مدى صحتها.
وهناك أمل في أن تساعد هذه الاكتشافات الحديثة في التقليل من خطر حدوث أوبئة المكورات السحائية، وتعتمد اللقاحات الحالية ضد المكورات السحائية على المحفظة عديدة السكريدات التي تحيط بالبكتيرة، وهي ليست فعالة في الأطفال الذين يتم تلقيحهم خلال برامج التلقيح الروتينية. فالحماية التي توفرها هذه اللقاحات للأطفال قصيرة الأجل، لذا فإن تلقيحهم في الفترات الخالية من الأوبئة لا يقيهم من الإصابة بالمرض خلال الموجة الوبائية التالية.
وقد يمكن التغلب على هذه المشكلة بتطبيق تقانة حديثة، يتم فيها الربط كيميائيا بين عديدة السكريدات المحفظية وبين حامل بروتيني protein carrierلصنع لقاح مترافق (مزدوج) conjugate. وإلى حد كبير، ثبت نجاح اللقاح المترافق (البروتين مع عديدة السكريدات) في استخدامه لدى الأطفال الصغار ضد المستدمية النزلية (هيموفيلوس إنفلونزا) Hemophilus influenzae ـ وهي بكتيرة أخرى مسببة لالتهاب السحايا. وقد شكلت منظمة الصحة العالمية (WHO) لجنة أبحاث لإنتاج واختبار لقاحات مترافقة (بروتينية ـ عديدة السكريدات) مشابهة ضد المجموعة المصلية A من المكورات السحائية. ومن الخصائص المثيرة الأخرى لهذه اللقاحات قدرتها على تقليل نسبة حَمْل الأشخاص الأصحاء للعامل المُمْرِض، وهي خاصية يمكنها أن تعوق عملية انتقال العامل الممرض، ومن ثم تقي الأفراد من الإصابة بالمرض.
وقد تقدم لنا هذه التبصرات، وغيرها، الوسائل المطلوبة لتلقيح وحماية المجموعات السكانية المتعرضة لخطر الإصابة بالأوبئة. لكن تبقى العقبات التي تواجه عمليات تصنيع لقاحات جديدة، وهي عقبات سياسية واقتصادية، إضافة إلى الصعوبات العلمية. فلا تزيد الميزانية الصحية السنوية في بعض الأقطار النامية على خمسة دولارات للفرد. لذا، هناك حاجة ملحة إلى معالجات (مقاربات) خلاّقة لعملية تصنيع اللقاحات في القريب العاجل. ونأمل أن يتم ترسيخ التعاون بين الشركات الصانعة للقاحات وبين هيئات الإغاثة الدولية وحكومات الأقطار النامية لحل هذه المشكلات.
وحتى الآن، مازال للكشف المبكر عن الأوبئة وشيكة الحدوث أهمية حيوية. فعلى الرغم من أن اللقاح الحالي لا يتيح مناعة طويلة الأجل، فإنه يمكن استخدامه خلال حملات التلقيح العاجلة أثناء انتشار الوباء. ويتم رسم الخطط لتوجيه حملات التلقيح اعتمادا على عدد حالات الإصابة المرضية في مجموعة سكانية معينة. وقد أنتج <T .J. بولمان> (من المعهد الوطني الهولندي للصحة العامة) أضدادا وحيدة النسيلة لاكتشاف نسائل المجموعة المصلية A من المكورات السحائية. وتقدم لنا أبحاثه طريقة أبسط وأسرع لتتبع هذه النسائل.
ويوضح انتشار النسيلة III-1 كيف أصبحت القرية العالمية مترابطة. وقد تمكنا من أن نُزيل حَمْل النسيلة III-1 من جزء ضئيل فحسب من حجاج الولايات المتحدة إلى مكة المكرمة. لكن يبدو أن عوامل اجتماعية ـ اقتصادية، لحسن الحظ، قد منعت هذه السلالة من التسبب في حدوث الوباء في الولايات المتحدة وأوروبا. إلا أننا لم نكن محظوظين بالدرجة نفسها في مواجهة الأمراض الأخرى، مثل مرض نقص المناعة المكتسب (الإيدز AIDS)، فلم تلاق إجراءات اختبار وحَجْر quarantining المسافرين أي قدر من النجاح حتى الآن، ومن الواضح أنها لن تنجح في المستقبل بالمثل. لذا سيكون بوسعنا حماية شعوب الأقطار النامية فقط بخلق الالتزام بالمنطرة (التقصي) monitoring وبالصحة العامة، لا سيما في الأقطار ذات الموارد الصحية المحدودة.
المؤلفان
Claire V. Broome – Patrick S. Moore
متخصصان في الصحة العامة والوقاية من الأمراض الخمجية. يشغل مور، حاليا، منصب أستاذ بكلية الصحة العامة التابعة لجامعة كولومبيا، وله اهتمام قديم بصحة اللاجئين وبفهم العملية الوبائية. وهو يستخدم حاليا التقنيات الجزيئية لدراسة المُمْرِضات الجديدة. وتشغل بروم منصب نائب مدير مراكز الوقاية من الأمراض ومكافحتها (CDC) ونائب المدير التنفيذي لوكالة المواد السامة وتسجيل الأمراض. وقد كانت، حتى عام 1990، تدير قسم التهاب السحايا والمُمْرِضات الخاصة في المركز الوطني للأمراض الخمجية.
مراجع للاستزادة
THE EPIDEMIOLOGY OF ACUTE BACTERIAL MENINGITIS IN TROPICAL AFRICA. B. M. Greenwood in Bacterial Meningitis. Edited by J. D. Williams and J. Burnie. Academic Press, 1987.
GLOBAL EPIDEMIOLOGY OF MENINGOCOCCAL DISEASE. Belljamin Schwartz, Patrick S. Moore and Claire V. Broome in Clinical Microbiology Reviews, Vol. 2, Supplement, pages 5118-5124; April 1989. MENINGOCOCCAL MENINGITIS IN SUB-SAHARAN AFRICA: A MODEL FOR THE EPIDEMIC PROCESS. Patrick S. Moore in Clinical Infectious Diseases, Vol. 14, No. 2, pages 515-525; February 1992.
Scientific American, November 1994