تبعث العلاجات الجينية التي تسمح للأطفال الصم بالسمع على الأمل- وتطرح العديد من الأسئلة
تتقصى أخبار العلوم إمكانية توسيع نجاحاته لتشمل أنواعاً أخرى من الصمم
حملت الأشهر القليلة الماضية أخباراً مشوقة وهي أنه، ولأول مرة، أتاحت تقنية العلاج الجيني Gene therapy استعادة السمع جزئياً لدى الأطفال المولودين بطفرات Mutations أدت إلى إصابتهم بالصمم. أعلنت شركة إيلي ليلي أند كو Eli Lilly & Co. في هذا الأسبوع، على سبيل المثال، أن صبياً من المغرب يعاني الصمم التام، تلقى علاجها كجزء من تجربة إكلينيكية (سريرية) في فيلادلفيا، ليكون بوسعه الآن سماع الأصوات. وصار بوسع ثلاثة أطفال من الصين -في أعمارٍ أصغر- وخضعوا لعلاج مماثل، التواصل شفهياً دون الاستعانة بقوقعاتهم المزروعة Cochlear implants. وكانت تفاصيل استعادتهم حاسة السمع، والتي غطتها الصحافة لأول مرة في أكتوبر 2023، قد استُعرِضت بالتفصيل في دورية ذا لانسيت The Lancet خلال الأسبوع الأخير من يناير 2024.
وقالت كارين أفراهام Karen Avraham، الاختصاصية بعلم الجينات: «إنه لإنجازٌ علمي خارق». ويتفق معها في الرأي لورانس لوستيغ Lawrence Lustig، اختصاصية الأنف والأذن والحنجرة والمعالج الجيني من جامعة كولومبيا Columbia University، الذي كان مختبره سبَّاقاً في اختبار التقنية نفسها على الفئران، وعقَّب قائلاً: «إلى جانب القوقعات المزروعة، لم نتوصل إلى أي علاجات ناجحة لمعالجة الصمم».
ويُتوقع ورود المزيد من الأخبار السارة حينما تُستعرض النتائج التي توصل إليها فريقان آخران مختصان بالعلاج الجيني، إلى جانب المزيد من البيانات الخاصة بتجارب شركة إيلي ليلي والفريق الصيني، خلال الاجتماع السنوي الذي تعقده رابطة أبحاث الأنف والأذن والحنجرة Association for Research in Otolaryngology في فبراير. تستعين هذه الجهود من شركات ومراكز أكاديمية على اختلافها بفيروس يقوم بغرز الجينOTOF نفسه في الأذن الداخلية Inner ear للأطفال، بحيث يمكن لما يُعرف بالخلايا الشعرية Hair cells، استشعار الصوت ونقله إلى الدماغ. هذا، وتُضاف علاجات الصمم الجديدة إلى سلسلة من النجاحات الأخيرة المحرزة في مجال العلاج الجيني، إلاْ أنها كذلك تطرح تساؤلاتٍ عدة.
ما نوع الصمم المعالج، وكيف يعمل العلاج؟
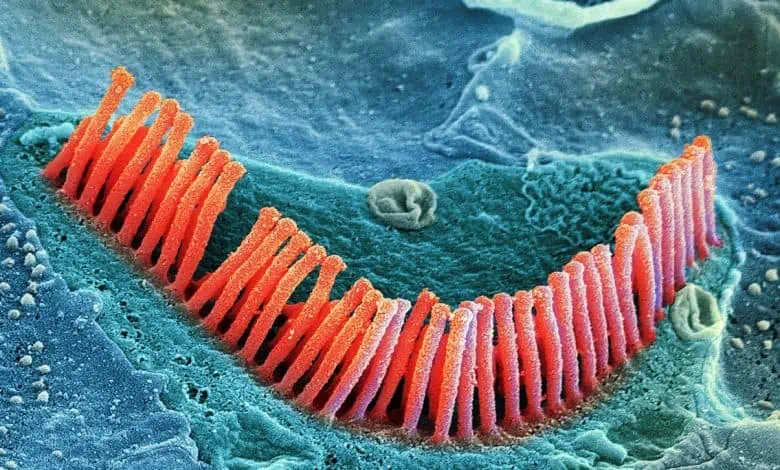
يُرمِّز (يشفِّر) Encodes جين OTOF بروتينا يدعى أوتوفيرلين Otoferlin، وهو ضروري لنقل الأصوات التي تتسبب بانحناء النتوءات الخشنة الكائنة على الخلايا الشعرية (خلايا الشعر) Hair cells للأذن. ومع ذلك، يولَد ما يقرب من 200,000 شخص حول العالم بنسختين معيبتين من هذا الجين، وهو ما يجعلهم صُمّاً، إلّا أنه يظل عندهم خلايا شعرية يحتمل أن تكون قادرة على العمل في حال توفر الناقل العصبي Neurotransmitter. يتلقى الأطفال حقنةً من فيروسين غير ضارين في القوقعة، يحمل كل منهما جزءا من تسلسل الجين OTOF. عندما يدخل كل فيروس إلى خلية شعرية ويطلق حمولته، يتشكل البروتين كاملاً في النهاية. والجين الكامل كبير جدا، إذ يبلغ طوله 6,000 قاعدة، ولا يمكن جمعه ضمن فيروس واحد من الفيروسات الغدانية (Adenovirus، اختصاراً: الفيروسات AAV)، وهو ما يُدعى بالناقل Vector، والمستعمل في العديد من العلاجات الجينية.
يختلف النهج الذي تحذوه الشركات في تصميمها للفيروسات AAV من شركة إلى أخرى بعض الشيء، وتختلف الكيفية التي يقسمون من خلالها الجين، إلاّ أن «الإستراتيجية العامة متماثلة إلى حدٍ كبير» كما يقول جيفري هولت Jeffrey Holt، عالم الأحياء العصبي والباحث في العلاج الجيني في مستشفى بوسطن للأطفال Boston Children’s Hospital، والذي لم يكن مشاركاً مع أي من هذه الفرق. وقد بدأت للتو التجارب الإكلينيكية لهذه العلاجات القائمة على «الفيروسات AAV المزدوجة»، وقد تكون نتائج ذا لانسيت The Lancet أول نجاحٍ أكلينيكي تنشر نتائجه، كما قال جيفري تشامبرلين Jeffrey Chamberlain، الباحث في العلاج الجيني بجامعة واشنطن University of Washington.
ما مدى نجاح العلاج، وإلى متى ستدوم أدلة التحسن؟
في ظرف شهرٍ واحد، استطاع الطفل المغربي البالغ من العمر 11 عاماً، والذي لم يكن عنده قوقعة مزروعة Cochlear implant، من سماع بعض الترددات مثله مثل شخصٍ طبيعي، بحسب ما أفادت به إيلي ليلي والشركة الشريكة Partner company أكيوس Akouos في هذا الأسبوع. غير أن الطفل، الذي يستخدم لغة الإشارة، لا يزال غير قادر على التكلم لأنه ليس بمقدور أدمغتنا اكتساب تلك القدرة بعد تجاوز سن الخامسة، مثلما ذكر الباحثون لصحيفة ذا نيويورك تايمز The New York Times.
أفادت التقارير أن خمسة من الأطفال الستة الذين شملتهم التجربة التي أجريت في جامعة فودان Fudan University، والذين حصل بعضهم على قوقعة مزروعة Cochlear implant في أحد الأذنين وهو ما منحهم سمعهم جزئيا، قد صاروا الآن قادرين على سماع الأصوات دون تشغيل تلك الأجهزة، وتحسّنت قدرتهم على النطق؛ إذ بوسع طفلين أصغر سناً الآن أن يسمعوا دون الاستعانة بقوقعة مزروعة. وذكرت شركة ريجينيرون للصناعات الدوائية Regeneron Pharmaceuticals أن سمع أحد الرضع ممن تلقوا العلاج OTOF-AAV شهد تحسناً، ومن المقرر أن تُقدم شركة أوتوفيو ثيرابيوتيكس Otovio Therapeutics الصينية تقريراً خلال الاجتماع حول تحسن حاسة السمع لدى مريضَين في مقتبل العمر.
من المتوقع أن يكون مستوى الأصوات التي سوف يسمعها الأطفال أكثر طبيعية من تلك التي تتيحها القوقعة المزروعة، وهو ما قد يؤدي إلى تحسنٍ في السمع. غير أن لوستيغ، المشارك في تجربة ريجينيرون Regeneron، يقول: «حتى يكبر هؤلاء الأطفال، لا أعتقد أننا سنحظى حقا بفهم أفضل» بمدى تحسن قدرتهم على فهم الكلام. ليس لخلايا الأذن الشعرية القدرة على الانقسام، لذا ينبغي على النسخ الجديدة من جين OTOF -المُحتواة ضمنها- أن تظل مواظبة وتستمر بإصدار التعليمات للخلايا من أجل إنتاج الأوتوفيرلين Otoferlin. ولكن، لا توجد طريقة لمعرفة إلى متى ستدوم أدلة التحسن دون جمعِ مزيدٍ من البيانات على مدى سنوات عديدة، بحسب ما قالته أفراهام. ويمكن للتعبير الجيني أن يتراجع بمرور الوقت، أو أن تطوِّر الأذن استجابةً مناعيةً تؤدي إلى تثبيطه.
ما اضطرابات الصمم الأخرى التي قد يمكن مداواتها بالعلاج الجيني؟
تسعى العلاجات الجينية إلى تحقيق أهداف محتملة أخرى، بما أن عدد الجينات التي يمكن لها أن تتسبب طفراتها بالصمم يفوق المئة جين. ولكن الباحثين يقولون إن تطوير هذه العلاجات سيستغرق وقتاً. من المرجح أن تتناول التجارب القادمة اضطرابات أخرى تظل فيها الخلايا الشعرية سليمة لمدة لا تقل عن بضع سنوات بعد الولادة. وتشمل تلك القائمة الصمم الناجم عن عيوب في الجينات مثل الجين TMRPSS3، فضلاً عن بعض أشكال متلازمة آشر Usher syndrome، وهو اضطراب يؤدي أيضاً إلى الإصابة بالعمى.
غير أن الثمرة الأهم ستكمن في التوصل إلى علاجٍ يصحح العيوب في الجين GJB2، والذي تُعزى إليه ما نسبته 30% من معظم حالات الصمم الوراثي ضمن بعض الشرائح السكانية. يُرمِّز الجين بروتيناً يدعى كونيكسين 26 (Connexin 26)، والذي يعمل على مساعدة أنواع مختلفة من الخلايا في القوقعة على التواصل من خلال إفراز البوتاسيوم. ومع ذلك، يعد اضطراباً عويصاً من منطلق العلاج الجيني؛ إذ لا يمكن الاعتماد على الفيروسات AAV حالياً لإضافة الجين المطلوب إلى تلك الخلايا فقط، دون إضافتها إلى خلايا أخرى في القوقعة. فإضافة بروتينات كونيكسين 26 للخلايا التي لا تعوزه يشبه «إحداثَ ثقبٍ» في الخلية على حد تعبير هولت. ويتابع قائلا: «ففي حال تواجد البروتين في خلية شعرية أو عصبية، فإنه سيولد بعض المشكلات». غير أن لوستيغ أبدى تفاؤله حيال التغلب على مختلف هذه التحديات، وأردفَ قائلاً: «بعدما حققنا الآن قصة نجاحٍ واحدة، سيتوفر المزيد من التمويل لبعض هذه المشروعات الأخرى».
ماذا عن الأطفال أو البالغين الصم، ممن لم يبقَ لديهم خلايا شعرية قابلة للإصلاح؟
قبل عقد من الزمن، حاولت شركة نوفارتس Novartis استخدام العلاج الجيني من أجل إعادة توليد الخلايا الشعرية لدى البالغين الذين يعانون فقدانا حادا في السمع نتيجة خسارتهم لتلك الخلايا بفعل التعرض للضوضاء أو المواد السامة. وتمثلت الفكرة في استخدام الفيروس AAV من أجل إيصال الجين إلى الخلايا القوقعية المجاورة، ليحرِّض بروتينه جيناتٍ أخرى قادرة على تحويل الخلايا المجاورة إلى خلايا شعرية.
أخفق هذا العلاج، ولعل السبب أنه كان لدى البالغين عدد ضئيل جدا من هذه الخلايا «الداعمة» Supporting بحسب ما يقوله لوستيغ، الباحث المشارك في التجربة. وفي مسعىً أحدث لإعادة توليد الخلايا الشعرية لدى البالغين، حقنت شركة تدعى فريكوينسي ثيرابيوتيكس Frequency Therapeutics مادة هلامية تحتوي على أدوية في محاولة لتحفيز الخلايا الداعمة على التحول إلى خلايا شعرية. غير أن سمع المرضى لم يتحسن مقارنة بالمشاركين الذين تلقوا دواءً غفلاً (وهمياً) Placebo، وأغلِقت الشركة في فبراير 2023.
يقول لوستيغ إن تحفيز إعادة نمو الخلايا الشعرية قد يكون أكثر تعقيداً مما كان يُظن، وأتبع قائلاً: «أعتقد أن تجارب إعادة التوليد هي الآن ذات أولوية ثانوية».
ما ملامح العلاج الجيني للصمم مستقبلاً؟
مع ظهور المزيد من العلاجات، يُأمَل في حال فشل حديثي الولادة في اجتياز اختبار السمع الروتيني عند الولادة، أن يُفحصوا للتحقق من وجود أسباب وراثية محتملة مثل الجين OTOF حتى يمكن معالجتهم فورا. يحلم بعض باحثي الصمم بعلاج الصمم الوراثي من الرحم في حال صار إجراء فحص جيني شامل للجنين جزءاً من الرعاية في فترة ما قبل الولادة.
غير يعارض بعض أفراد مجتمع الصم تلك «العلاجات» التي يرونها تطمس ثقافة الصم؟
يقول هولت إنه على دراية جيدة بتلك الحجج، وأتبع قائلاً: «وما نود القيام به هو توفير خيارات عدة. لا نريد فرض ذلك على أي شخص». وتشير أفراهام إلى أن الغالبية الساحقة من الأطفال الصم يولدون لأبوين قادرين على السمع، وأنهم «مستعدون لفعل أي شيء لتزويد أطفالهم بالقدرة على السمع».
بقلم: جوسيلين كايسر





